题目内容
下列离子能在pH=11的溶液中大量共存的是( )
| A、CO32-、K+、Cl-、Ca2+ |
| B、K+、NO3-、Na+、OH- |
| C、H+、Ba2+、Cl-、SO42- |
| D、K+、OH-、SO42-、Cu2+ |
考点:离子或物质的共存问题,溶液的酸碱性与pH值的关系
专题:物质的分离、除杂、提纯与共存问题
分析:pH为11的水溶液显碱性,水溶液中含有大量的OH-.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存,据此进行分析判断即可.
解答:解:pH为11的水溶液显碱性,水溶液中含有大量的OH-.
A、CO32-、Ca2+两种离子能结合成碳酸钙沉淀,不能大量共存,故选项错误;
B、四种离子间不能结合成沉淀、气体或水,能在碱性溶液中大量共存,故选项正确;
C、Ba2+、SO42-两种离子能结合成硫酸钡沉淀,氢离子不能在碱性溶液中大量共存,故选项错误;
D、Cu2+、OH-两种离子能结合成氢氧化铜沉淀,不能大量共存,故选项错误;
故选B.
A、CO32-、Ca2+两种离子能结合成碳酸钙沉淀,不能大量共存,故选项错误;
B、四种离子间不能结合成沉淀、气体或水,能在碱性溶液中大量共存,故选项正确;
C、Ba2+、SO42-两种离子能结合成硫酸钡沉淀,氢离子不能在碱性溶液中大量共存,故选项错误;
D、Cu2+、OH-两种离子能结合成氢氧化铜沉淀,不能大量共存,故选项错误;
故选B.
点评:本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;还要注意是在碱性溶液中共存.

练习册系列答案
相关题目
某学生用量筒量取液体的体积,量筒放平稳且面对刻度线,初次仰视凹液面的最低点读数为19mL,倾出部分液体后,俯视液体凹液面的最低处读数为10mL,则实际该学生倾出液体的体积是( )mL.
| A、9 | B、大于9 |
| C、小于9 | D、无法判断 |
下列微粒符号中,“2”对含义理解正确的是( )
| A、2Cu中的“2”表示2个铜元素 | ||
| B、H2S中的“2”表示一个硫化氢分子中含有2个硫原子 | ||
| C、Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷 | ||
D、Al2(S
|
下列关于燃烧现象的描述,正确的是( )
| A、铁丝在空气中剧烈燃烧,火星四射 |
| B、红磷在空气中燃烧产生大量白雾 |
| C、木炭在氧气中燃烧产生二氧化碳 |
| D、硫在空气中燃烧发出微弱的淡蓝色火焰 |
节约用水和合理开发利用水资源是每个公民应尽的责任和义务,你认为下列做法与之不相符的是( )
| A、淘米水用来浇花 |
| B、向河道中丢弃生活垃圾 |
| C、合理施用农药、化肥,以减少水体污染 |
| D、加强工业废水的排放监控,坚持达标排放 |
必须依靠其他试剂才能区别的一组溶液是( )
| A、FeCl3、NaOH、NH4Cl、ZnSO4 |
| B、浓硫酸、浓盐酸、K2CO3、AgNO3 |
| C、Na2SO4、BaCl2、K2CO3、KNO3 |
| D、BaCl2、CuSO4、NaOH、NaCl |
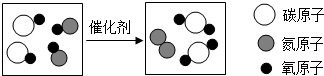 如图是治理汽车尾气反应的微观过程,图中单质是
如图是治理汽车尾气反应的微观过程,图中单质是