题目内容
3.在实验室常用以下装置制取气体.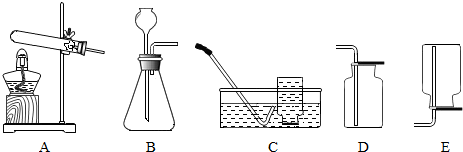
(1)用氯酸钾和二氧化锰制氧气的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,发生装置应选(填字母序号,下同)A;收集装置可选C或D.
(2)用石灰石和稀盐酸制二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,发生装置应选B; 证明集满的方法是燃着木条在集气瓶口熄灭.
(3)收集氧气可选用的装置之一是C(或D),依据是氧气不易溶于水(或氧气的密度比空气略大).
分析 (1)根据反应原理以及制取和收集方法的选择依据来分析;
(2)根据实验室中制取二氧化碳的反应原理和反应条件来选择反应的发生装置,根据二氧化碳的密度及水溶性来选择收集装置;由二氧化碳的化学性质确定其验满方法.
(3)根据氧气的密度和溶水性选择收集装置.
解答 解:(1)实验室用氯酸钾和二氧化锰制取氧气需要加热,应该用A装置作为发生装置;氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;氧气的密度比空气大,且不易溶于水,故填:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;A;C或D;
(2)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.所以应该选择B装置来制取二氧化碳气体;二氧化碳密度比空气大,能溶于水,所以应该选择D装置来收集二氧化碳.检验二氧化碳是否收集满时,将燃着的木条放在集气瓶口,若木条熄灭,说明已集满.故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;B;燃着木条在集气瓶口熄灭;
(3)氧气的密度大于空气的密度,而且不易溶于水,所以可用排水法和排空气法收集.故填:C(或D);氧气不易溶于水(或氧气的密度比空气略大).
点评 此题重在考查根据物质的反应物和反应条件选取装置.会从题干信息中找突破口,找出反应物和生成物,写化学方程式.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
18.下列变化过程与氧气无关的是( )
| A. | 动物呼吸 | B. | 生石灰变质 | C. | 食物腐烂 | D. | 木材燃烧 |
15.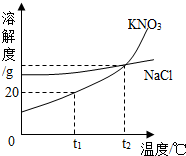 如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
 如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )| A. | NaCl的溶解度不受温度的影响 | |
| B. | t1℃时,100gKNO3饱和溶液含有KNO320g | |
| C. | t2℃时,NaCl与KNO3饱和溶液中溶质的质量分数相等 | |
| D. | 温度在t1℃到t2℃之间时,无法比较KNO3和NaCl溶解度 |
11.下列说法中,不正确的是( )
| A. | 在其它条件不变时,CO2的溶解度随压强的升高而增大 | |
| B. | 碳具有可燃性,在常温下其化学性质比较活泼 | |
| C. | 一氧化碳和木炭都具有还原性 | |
| D. | CO2能溶于水,CO难溶于水 |
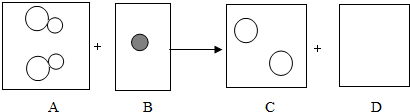
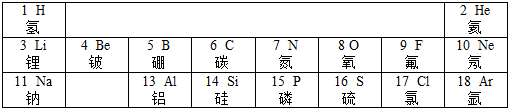
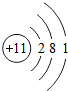 ,该原子在化学反应中易失去(填“得到”或“失去”)电子.
,该原子在化学反应中易失去(填“得到”或“失去”)电子.