题目内容
14. 某同学发现张大爷家菜园中的蔬菜生长迟缓,便帮他购买施用了一包化肥,右图为该包化肥的外包装标签上的部分说明,请仔细阅读标签并回答下列问题(商品的标签或说明书上常常用质量分数来表示某物质的成分或纯度):
某同学发现张大爷家菜园中的蔬菜生长迟缓,便帮他购买施用了一包化肥,右图为该包化肥的外包装标签上的部分说明,请仔细阅读标签并回答下列问题(商品的标签或说明书上常常用质量分数来表示某物质的成分或纯度):(1)硝酸铵中含有铵根离子和硝酸根离子,硝酸根离子中氮元素的化合价为+5.
(2)硝酸铵中氮元素和氢元素的质量比为7:1.
(3)硝酸铵中氮元素的质量分数为35%.因此证明这包氮肥包装标签的说明有(填“有”或“没有”)虚假之处.
(4)经化验证明这包化肥的纯度为96%(其余成分中无氮元素),则这包化肥中共含有16.8kg的氮元素.(请写出计算过程)
分析 (1)硝酸铵中,铵根中的氮元素的化合价为-3,硝酸根中的氮元素化合价为+5,据此解答.
(2)元素的质量比就是相对原质量乘以原子个数之比,据此解答.
(3)根据物质中某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{化合物的相对分子质量}$×100%,进行解答.
(4)化肥中氮元素的质量=硝酸铵的质量×化肥的纯度×硝酸铵其氮的质量分数.
解答 解:(1)硝酸铵中,铵根中的氮元素的化合价为-3,硝酸根中的氮元素化合价为+5,故填:+5.
(2)硝酸铵NH4NO3中氮元素和氢元素的质量比为:14×2:1×4=7:1,故填:7:1.
(3)硝酸铵的化学式为NH4NO3;则氮元素的质量分数为:$\frac{氮元素的相对原子质量×氮原子的个数}{硝酸铵的相对分子质量}$×100%=$\frac{28}{80}$×100%=35%;由此证明这包氮肥包装标签的说明
有虚假之处,故填:35%;有.
(4)这包化肥中氮元素的质量=50kg×96%×35%=16.8kg.
故填:16.8.
点评 本题考查了根据化学式的有关计算,完成此题,可以依据有关的公式进行.

练习册系列答案
相关题目
4.下列人体所缺元素与引起的健康问题关系错误的是( )
| A. | 缺铁会引起贫血 | B. | 缺碘会引起龋齿 | ||
| C. | 缺钙会引起骨质疏松 | D. | 缺锌会引起发育停滞得侏儒症 |
2.如图为某反应前后分子种类变化的微观示意图,其中不同的球代表不同种原子.下列说法中,不正确的是( )


| A. | 分子在化学变化中可分 | |
| B. | 原子在化学变化中不可分 | |
| C. | 此反应一定有单质生成 | |
| D. | 参加反应的两种分子的个数比为1:1 |
19.某同学设计下表所示实验,探究金属铜对过氧化氢分解速率的影响.
回答下列问题:
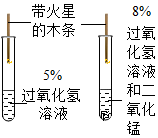
(1)写出铜加入过氧化氢溶液中反应的符号表达式2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑
(2)仪器②中实验的目的是和①作对比(对照).
(3)根据上述实验,可以得出的结论是金属铜对过氧化氢溶液分解速率有加快的作用.
(4)如果用上述实验探究铜是不是过氧化氢分解的催化剂,需要对上述实验方案进行补充.验证铜的质量和化学性质在反应前后都没有变化才能证明铜是过氧化氢分解的催化剂.若铜是过氧化氢分解的催化剂,操作步骤3中两支试管最终收集到的氧气体积左试管等于右试管(填多于、少于或等于).
(5)某学习小组探究催化剂二氧化锰的用量对反应速率的影响.他们做了这样一组实验:每次用30mL10%的过氧化氢溶液,采用不同量二氧化锰粉末做催化剂,测定各收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
请分析表中数据,得出结论:
①由表格可知二氧化锰的用量对双氧水分解速率影响规律是在一定范围内,二氧化锰的用量越多,反应速率越快
②二氧化锰用量超出一定范围后,二氧化锰的量对反应速率的影响不明显.
| 操作 | 装置 | 现象 |
| 1.取一小块铜丝网,卷成筒形,固定在铜丝上. |  | |
| 2.分别向①和②中注入15mL、30%的过氧化氢,并放入盛有热水的③中. |  | 约1min后可观察到①和②中都有少量气泡产生. |
| 3.把铜丝网插入①中. | 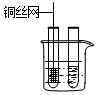 | ①中有大量气泡产生,5min后不再有气泡产生;此时②中仍然不断有少量气泡产生. |
(1)写出铜加入过氧化氢溶液中反应的符号表达式2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑
(2)仪器②中实验的目的是和①作对比(对照).
(3)根据上述实验,可以得出的结论是金属铜对过氧化氢溶液分解速率有加快的作用.
(4)如果用上述实验探究铜是不是过氧化氢分解的催化剂,需要对上述实验方案进行补充.验证铜的质量和化学性质在反应前后都没有变化才能证明铜是过氧化氢分解的催化剂.若铜是过氧化氢分解的催化剂,操作步骤3中两支试管最终收集到的氧气体积左试管等于右试管(填多于、少于或等于).
(5)某学习小组探究催化剂二氧化锰的用量对反应速率的影响.他们做了这样一组实验:每次用30mL10%的过氧化氢溶液,采用不同量二氧化锰粉末做催化剂,测定各收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化锰用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 时间(秒) | 22 | 13 | 12 | 10 | 9 | 8 | 5 | 3 | 3 | 3 |
①由表格可知二氧化锰的用量对双氧水分解速率影响规律是在一定范围内,二氧化锰的用量越多,反应速率越快
②二氧化锰用量超出一定范围后,二氧化锰的量对反应速率的影响不明显.
4.某油井燃烧,上空浓烟滚滚,造成严重的大气污染.你分析浓烟的主要污染成分是( )
| A. | 甲烷 | B. | 二氧化碳 | C. | 炭黑 | D. | 一氧化碳 |