题目内容
6. 近日,毒胶囊事件被推倒舆论的浪尖上.毒胶囊中铬超标,从元素周期表中查到的铬元素相关信息如右图所示.下列说法中正确的是A
近日,毒胶囊事件被推倒舆论的浪尖上.毒胶囊中铬超标,从元素周期表中查到的铬元素相关信息如右图所示.下列说法中正确的是AA.铬的元素符号是Cr B.中子数为24
C.原子质量为52.00 D.铬元素是金属元素.
分析 由上图铬元素在元素周期表中的说明示意图,可得的信息为:原子序数、相对原子质量、核内质子数、核外电子数、元素种类等.
解答 解:A.右上角的符号即为其元素符号,为Cr,故正确;
B.左上角的24为其原子序数,即核电荷数或质子数,而不是中子数,故错误;
C.根据元素周期表中铬元素的相关信息:相对原子质量为52.00,而不是原子的实际质量,故错误;
D.根据化学元素汉字名称的偏旁可辨别元素的种类,可知铬元素是金属元素.
故选A.D选项可以为:铬元素是金属元素.
点评 本题考查了元素周期表的应用,完成此题,可以依据元素周期表的意义进行.

练习册系列答案
相关题目
14.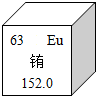 稀土元素是一类有重要用途的资源,铕是一种稀土元素,如图是元素周期表中铕元素的相关信息,下列说法正确的是( )
稀土元素是一类有重要用途的资源,铕是一种稀土元素,如图是元素周期表中铕元素的相关信息,下列说法正确的是( )
 稀土元素是一类有重要用途的资源,铕是一种稀土元素,如图是元素周期表中铕元素的相关信息,下列说法正确的是( )
稀土元素是一类有重要用途的资源,铕是一种稀土元素,如图是元素周期表中铕元素的相关信息,下列说法正确的是( )| A. | 铕属于非金属元素 | B. | 铕的原子序数是63 | ||
| C. | 铕原子中的中子数是63 | D. | 铕的原子质量是152.0 |
1.通过实验可以获取证据,得出结论.下列做法中不能获得明显证据的是( )
| A. | 为了证明氢氧化钠溶液呈碱性,在其溶液中滴加稀盐酸 | |
| B. | 为了证明铁的金属活动性比铜强,可将铁丝浸入到氯化铜溶液中 | |
| C. | 为了说明盐溶液不一定都呈中性,在碳酸钠溶液中滴加酚酞试液 | |
| D. | 为了证明汗水中含有Cl-,加入含稀硝酸的硝酸银溶液 |
18.四氧化三铁可用于医疗器械、电子等工业.某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验.
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液.
(3)制备Fe3O4的实验流程如图:

【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4(写一个即可).
(2)操作a的名称为过滤.该操作需要的玻璃仪器有烧杯、玻璃棒、漏斗等.
(3)溶液3所含溶质的主要成分为硫酸亚铁.
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
| Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
(3)制备Fe3O4的实验流程如图:

【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4(写一个即可).
(2)操作a的名称为过滤.该操作需要的玻璃仪器有烧杯、玻璃棒、漏斗等.
(3)溶液3所含溶质的主要成分为硫酸亚铁.