题目内容
16.碳酸钙是一种白色固体,可溶于稀盐酸并产生无色气体.某同学想知道稀盐酸中的哪种粒子(H2O、H+、Cl-)能使碳酸钙溶解并产生无色气体.请你和同学们一起通过如图所示的四个实验完成这次探究活动: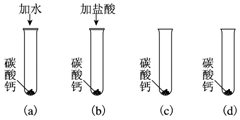
(1)你提出的假设是稀盐酸中的H+能使CaCO3溶解并产生无色气体;
(2)通过实验(a)可以证明H2O不能使CaCO3溶解并产生无色气体;
(3)要证明另外两种粒子能否溶解碳酸钙并产生无色气体,还需要进行实验(c)和(d),在(c) 和(d)中应分别加入硝酸和氯化钠溶液;
(4)你的探究结果为H+能使CaCO3溶解并产生无色气体.
分析 根据碳酸钙能与盐酸反应生成二氧化碳气体,要探究是稀盐酸中的哪种粒子(H2O、H+、Cl-)能使碳酸钙溶解并产生无色气体,需排除一些离子的干扰,设计实验时要注意控制变量进行分析.
解答 解:(1)碳酸盐与酸反应生成气体,是与酸中的氢离子结合反应生成了二氧化碳;
(2)向a中加水,碳酸钙不溶解也无气体产生,说明通过实验a可以证明:H2O不能使CaCO3溶解并产生无色气体;
(3)要证明是否是氢离子使碳酸钙溶解并产生气体,需加入含氢离子的物质,如硝酸,要证明是否是氯离子使碳酸钙溶解并产生气体,需加入含氯离子的物质,如氯化钠溶液;
(4)根据实验现象可知是氢离子使碳酸钙溶解并产生气体.
故答案为:(1)稀盐酸中的H+能使CaCO3溶解并产生无色气体;
(2)H2O不能使CaCO3溶解并产生无色气体;
(3)硝酸,氯化钠溶液;
(4)H+能使CaCO3溶解并产生无色气体.
点评 本题考查了碳酸钙与酸反应的实质,完成此题,要注意设计实验时变量的控制以及归纳法的应用.

练习册系列答案
相关题目
6.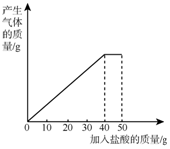 石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.
石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.
请计算:
(1)由图象可知,第四次加入10g盐酸后,碳酸钙固体又反应掉4克.
(2)完全反应后产生的二氧化碳.
(3)所加盐酸的溶质质量分数.
 石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.
石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象.| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 10 | 10 | 10 |
| 剩余固体的质量/g | 16 | 12 | 8 |
(1)由图象可知,第四次加入10g盐酸后,碳酸钙固体又反应掉4克.
(2)完全反应后产生的二氧化碳.
(3)所加盐酸的溶质质量分数.
11.为了探究影响固体溶解性的因素,某同学实际了如下三组实验
(1)分析上表,第一组实验研究的因素是溶剂种类;
(2)有上述实验可知,影响固体溶解性的因素是①②④;
①温度②加入溶剂种类③加入溶剂质量④假如固体种类⑤加入固体质量
(3)在第二组试验中,该同学按照如下步骤进行实验(假设溶液损失不计)
①用电子天平称取10.0g的硝酸钾,放入烧杯中;
②量取10.0ml水,倒入上述烧杯中,称量烧杯、硝酸钾和谁的总质量为m1g;
③胶版纸硝酸钾不在溶解为止;
④过滤,称量所得硝酸钾溶液和少北的总质量为m2g;
⑤计算:m1-m2=6.9g(结合第二组实验数据进行分析).
将溶质改为食盐,重复上述步骤进行试验.由实验可知,20℃是食盐的溶解性>(填“>”、“=”或“<”)硝酸钾的溶解性.
(4)根据上述实验,以下推论正确的是AD.
A.20℃时,氯化钠的溶解度为36g
B.20℃时,硝酸钾饱和溶液的溶质质量分数为31%
C.第三组实验中的硝酸钾溶液为80℃时的饱和溶液
D.20℃的任意一杯饱和硝酸钾溶液中,溶质与溶剂的质量比一定相等.
| 因素 | 第一组 | 第二组 | 第三组 | ||
| 实验温度 | 20℃ | 20℃ | 20℃ | 20℃ | 80°C |
| 加入溶剂种类 | 水 | 酒精 | 水 | 水 | 水 |
| 加入溶剂质量 | 20g | 20g | 10g | 10g | 10g |
| 加入固体种类 | 硝酸钾 | 硝酸钾 | 硝酸钾 | 食盐 | 硝酸钾 |
| 加入固体质量 | 10g | 10g | 10g | 10g | 10g |
| 溶解固体质量 | 6.2g | 0g | 3.1g/ | 3.6g | 10g |
(2)有上述实验可知,影响固体溶解性的因素是①②④;
①温度②加入溶剂种类③加入溶剂质量④假如固体种类⑤加入固体质量
(3)在第二组试验中,该同学按照如下步骤进行实验(假设溶液损失不计)
①用电子天平称取10.0g的硝酸钾,放入烧杯中;
②量取10.0ml水,倒入上述烧杯中,称量烧杯、硝酸钾和谁的总质量为m1g;
③胶版纸硝酸钾不在溶解为止;
④过滤,称量所得硝酸钾溶液和少北的总质量为m2g;
⑤计算:m1-m2=6.9g(结合第二组实验数据进行分析).
将溶质改为食盐,重复上述步骤进行试验.由实验可知,20℃是食盐的溶解性>(填“>”、“=”或“<”)硝酸钾的溶解性.
(4)根据上述实验,以下推论正确的是AD.
A.20℃时,氯化钠的溶解度为36g
B.20℃时,硝酸钾饱和溶液的溶质质量分数为31%
C.第三组实验中的硝酸钾溶液为80℃时的饱和溶液
D.20℃的任意一杯饱和硝酸钾溶液中,溶质与溶剂的质量比一定相等.
1.2016年6月9日12时杭州市环保局监测:杭州市空气质量指数67,空气质量级别Ⅱ级,空气质量良,空气首要污染物为可吸入颗粒物.下列有关空气各成分的说法正确的是( )
| A. | 氧气的化学性质比较活泼,属于可燃物 | |
| B. | 氮气的化学性质不活泼,可用于食品防腐 | |
| C. | 空气是由氮气、氧气、稀有气体、二氧化碳、氢气等物质组成的混合物 | |
| D. | 二氧化碳在空气中含量增多会引起温室效应,属于空气污染物 |
8.下列物质的化学式与名称表示一致并且书写正确的是( )
| A. | NH4HCO3--碳酸氢氧 | B. | CaO--熟石灰 | ||
| C. | NaOH--纯碱 | D. | CO(NH2)2--尿素 |
5.2017年我国在可燃冰开采技术上取得了世界性的突破.可燃冰分解出的甲烷属于( )
| A. | 混合物 | B. | 单质 | C. | 氧化物 | D. | 有机物 |
6.氯化钠的下列用途中,主要反映其具有杀菌防腐作用的是( )
| A. | 制生理盐水 | B. | 作调味剂 | C. | 腌制鱼肉 | D. | 制取氢氧化钠 |