题目内容
6. 雨、雪在形成和降落过程中可吸收、溶解空气中SO2及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨.请回答下列有关酸雨的问题:
雨、雪在形成和降落过程中可吸收、溶解空气中SO2及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨.请回答下列有关酸雨的问题:| 实验序号 | X的用量/g | Y的用量/g | 生成X2Y的质量/g |
| 1 | 6.4 | 1.8 | 7.2 |
| 2 | 9 | 3.6 | 12.0 |
A.蓝色石蕊试纸 B.紫色石蕊溶液 C.无色酚酞试剂 D.pH试纸
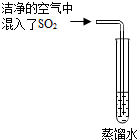
(2)已知 CO2的饱和溶液常温下pH不小于 5.6.通常空气中CO2的含量大于SO2的含量,但人们反而将空气中的 SO2认定为形成酸雨的主要原因之一.有同学想通过如图实验寻找证据,你认为下一步的实验步骤是测定溶液的酸碱度,只要出现pH值小于5.6的实验结果,就可认定SO2溶于水有形成酸雨的可能.
(3)已知SO2与 CO2有许多化学性质是相似的.亚硫酸钙(CaSO3)是白色、难溶于水但可溶于酸的固体.某同学向一酸雨样品中滴加 CaCl2溶液(如图),观察到没有浑浊现象,继续滴入NaOH溶液后即有白色沉淀产生.则在以上过程中不可能发生的化学反应是A
A SO2+CaCl2+H2O═CaSO3↓十2HCl.
B.SO2+2NaOH═Na2SO3+H2O
C. Na2SO3+CaCl2=CaSO3↓+2NaCl
D.H2SO3+2NaOH=Na2SO3+2H2O
E.SO2+H2O═H2SO3.
分析 (1)依据酸雨是pH小于5.6的降水可知要想证明是否是酸雨则要测定溶液的pH,据此分析即可.
(2)依据题干信息结合设计的实验可知,只要是证明亚硫酸的溶液pH能小于5.6即可完成相关的验证.
(3)依据对实验过程的叙述结合酸雨的成分和物之间的反应规律进行判断即可;
解答 解:
(1)因为酸雨是pH小于5.6的降水,所以要想证明是否是酸雨则要测定溶液的pH.
A、蓝色石蕊试纸是检验溶液酸性时常用的试纸,不能准确测量溶液酸碱度;
B、紫色石蕊溶液只能检验溶液的酸碱性,不能检测溶液的酸碱度;
C、无色酚酞试剂只能检验溶液的酸碱性,不能检测溶液的酸碱度
D、pH试纸能较准确地测量溶液的酸碱强弱的程度,所以检验某地是否下酸雨可利用pH试纸进行测量;
(2)二氧化硫溶于水会生成亚硫酸,二氧化碳溶于水会生成碳酸,而CO2的饱和溶液常温下pH不小于 5.6,所以要想证明二氧化硫是形成酸雨的主要成分,只要证明实验中亚硫酸的溶液pH能小于5.6即可.
(3)某同学向一酸雨样品中滴加 CaCl2,溶液未观察到有浑浊现象,说明没有发生A反应,因为A反应进行时会有白色沉淀产生,能溶于HCl,所以两者也不可能同时生成,由于二氧化硫和二氧化碳性质相似,所以B反应能够发生,继续滴入NaOH溶液后即有白色沉淀产生,说明发生了C反应,同时溶液中含有的亚硫酸也可与氢氧化钠发生中和反应,所以D反应可能发生;
答案:
(1)D
(2)溶液的酸碱度;pH值小于5.6
(3)A
点评 此题是一道与酸雨相关的考查题,涉及到酸雨的形成及实验验证,借助题干信息结合相关的所学知识是解题的关键所在;

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
16.将下列各组内的二种物质同时放入水中,能得到无色透明溶液的是( )
| A. | FeCl3、KOH | B. | K2SO4、BaCl2 | C. | CuSO4、HCl | D. | NaCl、KOH |
17.下图是某兴趣小组设计的四个实验装置,其中实验操作设计正确的是( )
| A. | 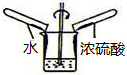 稀释浓硫酸 | B. |  探究可燃物燃烧的条件 | ||
| C. |  验证质量守恒定律 | D. | 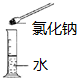 配制氯化钠溶液 |
14.不需要其它试剂就能区别的一组溶液是( )
| A. | FeCl3 NaOH KCl Ba(NO3)2 | B. | NaCl Na2CO3 KNO3 HCl | ||
| C. | Na2SO4 BaCl2 K2CO3 KNO3 | D. | BaCl2 CuSO4 NaOH NaCl |
1.以下几种实验操作,不正确的是( )
| A. | 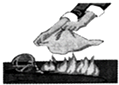 酒精灯失火用湿抹布扑盖 | B. |  将NaCl倒入量筒中配制溶液 | ||
| C. |  加碱研磨后闻气味鉴别铵态氮肥 | D. | 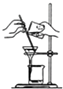 粗盐提纯过滤 |
18. 如图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )
如图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )
 如图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )
如图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )| A. | t1℃时,将40克B物质溶解在60克水中,溶质的质量分数为40% | |
| B. | t2℃时,三种物质的溶解度由大到小的顺序为:A>B>C | |
| C. | 要将C的不饱和溶液转化为饱和溶液可以采取升温的方法 | |
| D. | 要使A从其浓溶液中析出,可采用冷却热饱和溶液法 |
16.房屋在新装修后,室内空气通常含有较多甲醛,住户要注意通风,以防中毒.下列关于甲醛(HCHO)的说法,正确的是( )
| A. | 甲醛是一种酸 | |
| B. | 甲醛是由氢元素、氧元素和碳元素组成的一种氧化物 | |
| C. | 甲醛有挥发性 | |
| D. | 甲醛分子中碳、氢、氧各原子的个数比为1:1:2 |
