题目内容
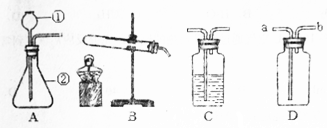
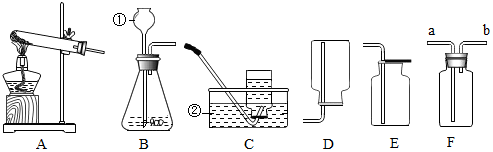
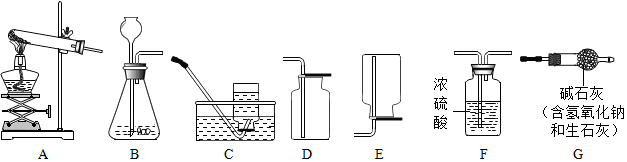
12.实验室制取气体常常用到下列装置,根据给出的装置回答下列问题: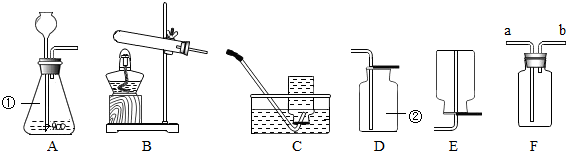
(1)写出标号仪器的名称:①锥形瓶;②集气瓶.
(2)若该实验选择装置A来制取氧气,请写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)用图F装置充满水来收集氧气,气体应从b(填“a”或“b”)端通入.
(4)某同学从上述装置图中选用适当装置成功的制备和收集了二氧化碳.选用的装置是AD
(填字母).该反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑,为了进一步验证产生的气体是二氧化碳该同学将气体通入图F装置中,则F装置中应加入的试剂为Ca(OH)2(填化学式).若在F装置中加入紫色石蕊试液,观察到的现象是有气泡产生,紫色石蕊溶液变红.
分析 (1)熟记仪器的名称;
(2)根据气体发生装置确定制取氧气的原理;
(3)根据氧气的密度比水小来分析;
(4)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;根据二氧化碳的检验方法以及二氧化碳的性质来分析.
解答 解:(1)仪器①是锥形瓶,②是集气瓶;故填:锥形瓶;集气瓶;
(2)装置A适用于固液常温下制取气体,即过氧化氢在二氧化锰的催化作用下分解为水和氧气;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)氧气的密度比水小,所以若用F装置充满水来收集氧气,氧气应从短管进入;故填:b;
(4)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,故选择装置A来制取;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳能使澄清石灰水变浑浊,所以用澄清石灰水来验证气体是否是二氧化碳;二氧化碳能与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色;故填:AD;CaCO3+2HCl═CaCl2+H2O+CO2↑;Ca(OH)2;有气泡产生,紫色石蕊溶液变红.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
12.将40克质量分数为10%的氢氧化钡溶液与20克质量分数为20%的盐酸溶液混合后,再加入下列物质:①AgNO3 ②Ba(NO3)2 ③NaOH ④Na2SO4,一定能发生反应的是( )
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①③④ |
4.下列有关物质制备的药品及原理完全正确的是( )
| A. | 实验室制二氧化碳:CaCO3+H2SO4=CaSO4+H2O+CO2↑ | |
| B. | 实验室制氧气:H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2↑+O2↑ | |
| C. | 实验室制氢气:Zn+2HCl=ZnCl2+H2↑ | |
| D. | 实验室模拟炼铁:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
 食品保鲜的措施有添加防腐剂、填充气体、放置干燥剂和脱氧保鲜剂等.
食品保鲜的措施有添加防腐剂、填充气体、放置干燥剂和脱氧保鲜剂等.