题目内容
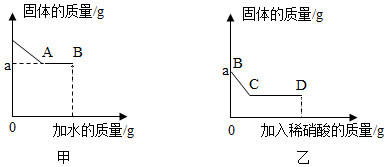
13. 金属铁及其化合物之间有如图转化关系.
金属铁及其化合物之间有如图转化关系.请回答下列问题:
(1)A是Fe2O3;B是FeCl3;
(2)写出A→B或A→C的化学反应方程式(任选一个):Fe2O3+6HCl=2FeCl3+3H2O或Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
(3)常温下,铁生锈的条件是铁接触空气中的水和氧气
(4)防止钢铁制品生锈常用的方法是(举一个实例):涂油或喷漆等.
分析 (1)根据铁锈的主要成分、氧化铁与盐酸反应、与硫酸反应的生成物回答本题;
(2)根据方程式的书写考虑;
(3)铁在与水和氧气并存时易生锈;
(4)防止金属锈蚀就是破坏铁生锈的条件.
解答 解;(1)铁锈的成分是氧化铁,氧化铁与盐酸反应生成氯化铁和水,氧化铁与硫酸反应生成硫酸铁和水,故B是氯化铁,故填;Fe2O3;FeCl3;
(2)氧化铁与盐酸反应生成氯化铁和水,与硫酸反应生成硫酸铁和水,故填:Fe2O3+6HCl=2FeCl3+3H2O或Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)常温下,铁接触空气中的水和氧气易生锈,故填:水;氧气;
(4)防止钢铁制品生锈可以在铁制品表面涂油或是刷漆,故填:涂油或喷漆等.
点评 解答本题关键是要知道铁锈的主要成分以及氧化铁与酸反应发生的是复分解反应,反应前后元素化合价不变.

练习册系列答案
相关题目
4.下列现象的微观解释,不正确的是( )
| A. | 水烧开后易把壶盖冲起--温度升高,分子变大 | |
| B. | 氢气和液氢都可作燃料--相同物质的分子,其化学性质相同 | |
| C. | 用警犬搜救地震中被埋人员--分子在不断运动 | |
| D. | 用水银温度计测量体温--温度升高,原子的间隔变大 |
1.2016年10月17日神舟十一号载人飞船成功发射,火箭所用的燃料液态偏二甲肼(C2H8N2)与N2O4发生的反应可写作:C2H8N2+2N2O4═3X↑+2CO2↑+4H2O↑其中X的化学式( )
| A. | N2 | B. | NO | C. | NO2 | D. | NH3 |
除去下列物质中混有的少量杂质,所用试剂或操作方法有明显错误的是( )
序号 | 物质 | 杂质 | 所用试剂和操作方法 |
A | NaOH溶液 | Na2SO4 | 加入适量的Ba(OH)2溶液、过滤 |
B | CO | 少量H2O和CO2 | 先通过浓硫酸,再通过氢氧化钠溶液 |
C | 铜粉 | CuO | 加入过量的稀盐酸,过滤 |
D | H2气体 | HCl | 通过足量NaOH溶液,干燥 |
A. A B. B C. C D. D
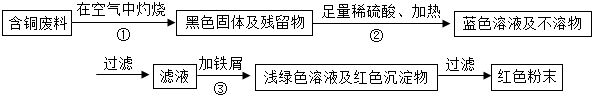

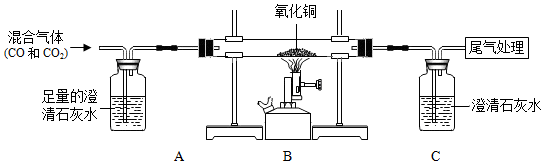
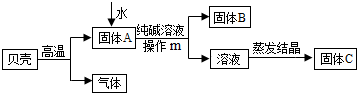
 化学材料和化学技术在家居生活中有着广泛的应用.
化学材料和化学技术在家居生活中有着广泛的应用.