题目内容
12.下列各组物质充分反应后,所得溶液质量相比反应前的溶液总质量减小的是( )| A. | 锌片浸入硫酸铜溶液中 | B. | 硝酸银溶液和氯化钠溶液 | ||
| C. | 二氧化硫通入氢氧化钠溶液中 | D. | 碳酸氢钠粉末加入稀盐酸 |
分析 首先确定溶液混合后是否发生反应,如果不反应,则溶液的质量保持不变;如果反应,若两种溶液反应后有沉淀或气体生成时会使溶液的质量减小,若反应前和反应后有固体或气体,可根据其质量差分析判断溶液质量的变化情况.
解答 解:A、锌片浸入硫酸铜溶液中,生成硫酸锌溶液和铜,锌的相对原子质量为65,生成的铜的相对分子质量为64,反应生成铜的质量小于所溶解锌的质量,所得溶液的质量比反应前溶液的总质量增加;故选项错误.
B、硝酸银溶液和氯化钠溶液反应生成氯化银沉淀和硝酸,两种溶液反应后有沉淀生成,则所得溶液的质量比反应前溶液的总质量减少,故选项正确.
C、二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水,反应后氢氧化钠溶液吸收了二氧化硫气体,所得溶液的质量比反应前溶液的总质量增大,故选项错误.
D、碳酸氢钠粉末加入稀盐酸生成氯化钠、水和二氧化碳,碳酸氢钠的相对分子质量为84,生成二氧化碳的相对原子质量为44,生成二氧化碳的质量小于参加反应的碳酸氢钠的质量,所得溶液的质量比反应前溶液的总质量增大;故选项错误.
故选:B.
点评 本题有一定难度,考查利用质量守恒定律来分析溶液质量的变化,确定反应前后溶液的种类、熟练应用质量守恒定律等是正确解答此类题的关键.

练习册系列答案
相关题目
4.发现问题小明同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥板上,发现大量气泡产生.
(1)提出问题:小明联想到自己曾经用二氧化锰作过氧化氢的催化剂,他想,水泥块能否作过氧化氢分解的催化剂呢?于是他到建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥,并进行以下探究.
(2)猜想:水泥块能作过氧化氢分解的催化剂.
(3)实验验证:
(4)结论:水泥块能加快过氧化氢的分解速率,故水泥块是过氧化氢分解的催化剂.
(5)讨论与反思:小冰认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,他觉得需要增加一个探究实验:水泥块在反应前后质量是否改变;
实验步骤:①准确称量水泥块质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、称量;④对比反应前后水泥块的质量;
(6)但老师指出:要证明小明的猜想,小冰的补充实验还是不足够,需要再补充一个探究实验:水泥块的化学性质在反应前后是否改变.
(1)提出问题:小明联想到自己曾经用二氧化锰作过氧化氢的催化剂,他想,水泥块能否作过氧化氢分解的催化剂呢?于是他到建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥,并进行以下探究.
(2)猜想:水泥块能作过氧化氢分解的催化剂.
(3)实验验证:
| 实验步骤 | 实验现象 | 实验结论 | |
| 实 验 一 | 将带火星的木条伸入装有过氧化氢溶液的试管中. | 木条不复燃 | 常温下过氧化氢溶液分解很慢. |
| 实 验 二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 加入水泥块能加快过氧化氢溶液的分解速率 |
(5)讨论与反思:小冰认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,他觉得需要增加一个探究实验:水泥块在反应前后质量是否改变;
实验步骤:①准确称量水泥块质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、称量;④对比反应前后水泥块的质量;
(6)但老师指出:要证明小明的猜想,小冰的补充实验还是不足够,需要再补充一个探究实验:水泥块的化学性质在反应前后是否改变.
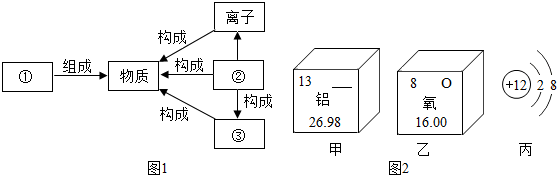
 ,丙图所示的粒子属于阳离子(填“原子”、“阳离子”或“阴离子”).
,丙图所示的粒子属于阳离子(填“原子”、“阳离子”或“阴离子”).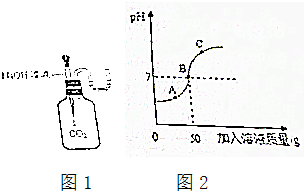 某兴趣小组的同学对氢氧化钠进行了以下探究活动.
某兴趣小组的同学对氢氧化钠进行了以下探究活动.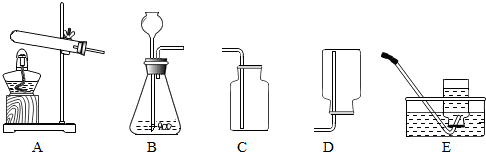
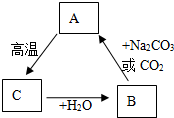 A、B、C是三种常见的含钙化合物,B的澄清溶液可用来检验二氧化碳气体,它们之间有如图所示的转化关系(部分产物略去):
A、B、C是三种常见的含钙化合物,B的澄清溶液可用来检验二氧化碳气体,它们之间有如图所示的转化关系(部分产物略去):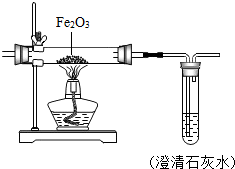 实验室常用如下装置图可做一氧化碳还原氧化铁的实验并检验反应生成的气体产物.
实验室常用如下装置图可做一氧化碳还原氧化铁的实验并检验反应生成的气体产物.