题目内容
9. 如图A、B、C为三种物质的溶解度曲线,据图回答:
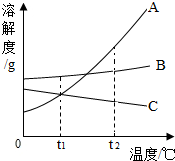
如图A、B、C为三种物质的溶解度曲线,据图回答:①t2℃时,A、B、C三种物质的溶解度由大到小顺序是ABC(或A>B>C);
②当A中含有少量B时为了得到纯净的A,可采用冷却热饱和溶液(或冷却结晶、降温结晶)的方法;
③若将t2℃三种物质的饱和溶液分别降到t1℃时,则三种溶液中溶质质量分数的大小关系是B>A>C.
分析 (1)根据某一温度时物质溶解度的比较方法考虑;
(2)根据固体物质从溶液中结晶析出的方法考虑.
(3)根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液质量;饱和溶液质量分数=$\frac{溶解度}{100g+溶解度}$×100%.
解答 解:(1)从t2℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t2℃时它们的溶解度大小顺序是A>B>C;
(2)如果溶解度受温度影响较大的物质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂;由于A物质的溶解度受温度影响较大,所以用冷却热饱和溶液或降温结晶的方法得到纯净的A.
(3)t2℃时三种物质的饱和溶液分别降到t1℃时,由于B的溶解度在t1℃时最大,因此溶质质量分数最大;
由于A在t1℃时的溶解度大于C在t2℃时的溶解度,因此A的质量分数大于C的质量分数.
故填:B>A>C.
故答案为:(1)ABC(或A>B>C);(2)冷却热饱和溶液(或冷却结晶、降温结晶);(3)B>A>C.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.解答本题关键是知道溶解度曲线表示的意义,知道溶解度如何比较大小,固体物质从溶液中结晶析出的方法.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
20.下列实验设计正确的是( )
| A. | 用食盐水除去热水瓶中的水垢 | |
| B. | 用淀粉溶液区别加碘食盐和无碘食盐 | |
| C. | 用肥皂水区分硬水和软水 | |
| D. | 用燃着的木条区别氮气和二氧化碳 |
4.类推是学习化学时常用的思维方式.以下类推结果正确的是( )
| A. | 物质和氧气发生的反应是氧化反应,所以发生氧化反应一定有氧气参加 | |
| B. | 碱溶液能使酚酞溶液变红,则能使酚酞溶液变红的物质一定是碱溶液 | |
| C. | 化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物 | |
| D. | 碳酸盐遇酸有气体产生,则与酸反应产生气体的一定是碳酸盐 |
14.2016年1月1日我国《环境保护法》颁布一周年,保护环境,人人有责,下列做法不合理的是( )
| A. | 提倡乘坐公交车、骑自行车或步行的出行方式 | |
| B. | 在生产和生活中提倡使用节能技术和节能用具 | |
| C. | 开发新能源,禁止开采和使用化石燃料 | |
| D. | 植树造林,严禁乱砍滥伐 |
1.下列属于有机合成材料的是( )
| A. |  涤纶 | B. |  铜丝 | ||
| C. |  棉花 | D. |  硅 |
18.清明时节,同学们相约外出踏青野炊.请用化学知识分析下列问题:
(1)野炊食谱如表所示:
从合理膳食角度来看,你认为食谱中还应添加C(填字母);
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)小滨用洗涤剂洗去手上的油渍,是利用了洗涤剂的乳化作用.
(1)野炊食谱如表所示:
| 主食 | 馒头 |
| 配菜 | 红烧肉、豆腐汤、牛肉干 |
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)小滨用洗涤剂洗去手上的油渍,是利用了洗涤剂的乳化作用.
19.下列图示的实验操作正确的是( )
| A. |  熄灭酒精灯 | B. |  取用碳酸钠固体 | C. | 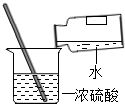 稀释浓硫酸 | D. | 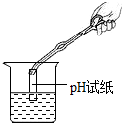 测溶液酸碱度 |