题目内容
6.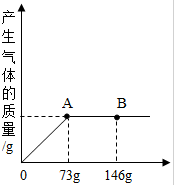 一烧杯中盛有30.8gBaCO3和BaCl2的粉末状混合物,向其中逐滴加入溶质的质量分数为10%的稀盐酸,产生气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答下列问题:
一烧杯中盛有30.8gBaCO3和BaCl2的粉末状混合物,向其中逐滴加入溶质的质量分数为10%的稀盐酸,产生气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答下列问题:(1)当滴入10%的稀盐酸至图中B点时,烧杯中溶液的pH大于7(填“大于”“小于”或“等于”;
(2)当滴入10%的稀盐酸73g时,烧杯中所得不饱和熔液中溶质的质量分数.(结果保留到0.1%)
分析 (1)根据当滴加稀盐酸至图中B点时,盐酸过量进行解答;
(2)根据当滴加了73g稀盐酸时,盐酸和碳酸钡恰好反应生成氯化钡,所以此时为不饱和的氯化钡溶液进行解答.
解答 解:(1)当滴加稀盐酸至图中B点时,盐酸过量,所以此时溶液中的溶质为CaCl2、HCl,溶液的PH>7;故填:大于;
(2)73g10%的稀盐酸中含HCl的质量是:73g×10%=7.3g
设参加反应的碳酸钡的质量为x,反应生成的氯化钡的质量为y,生成二氧化碳为z
BaCO3+2HCl=BaCl2+CO2↑+H2O
197 73 208 44
x 7.3g y z
$\frac{197}{x}=\frac{73}{7.3g}=\frac{208}{y}$=$\frac{44}{z}$
x=19.7g,y=20.8g,z=4.4g
所得不饱和熔液中溶质的质量分数$\frac{(30.8g-19.7g)+20.8g}{30.8g+73g-4.4g}$×100%=32.1%
答:所得不饱和熔液中溶质的质量分数32.1%.
点评 溶液和化学反应融合的题目,是综合性的题型,要求比较高.通常学生在计算时常常会忽视了实际参加反应的是溶液中溶质的质量,这就要求学生足够细心、会分析、且条理分明.

练习册系列答案
相关题目
16.下列物质的分类正确的是( )
| A. | 钢---单质 | B. | 氯酸钾------氧化物 | ||
| C. | 石灰水----碱 | D. | 硫酸铜---盐 |
11.下列对实验对象的描述,正确的是( )
| A. | 硫在氧气中燃烧,产生微弱的淡蓝色火焰 | |
| B. | 电解水时与正极相连的一端产生的气体体积是负极的2倍 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 红磷在空气中燃烧,产生大量烟雾,生成P2O5 |
 Cl-;
Cl-;