题目内容
12.化学是一门以实验为基础的科学,请结合图示回答问题:
(1)写出仪器①、②的名称,①长颈漏斗,②量筒.
(2)小杜同学准备用高锰酸钾制取并收集一瓶纯净的氧气,选择了AF(选填装置字母),作为发生装置,他选择的依据是固体需要加热制气体,该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,若还想利用H装置收集一瓶干燥的氧气,则氧气应从m端进入(填“m”或“n”)
(3)小彭同学设计了如图2所示装置验证二氧化碳的性质,当通入二氧化碳一段时间后,用化学方程式解释甲装置中颜色变化的原因是CO2+H2O=H2CO3,小张同学将变红的甲装置取下,放在酒精灯上充分加热,她看到的现象是红色又变紫色.乙装置中澄清石灰水变浑浊,反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
(4)小查同学在实验室用锌粒和稀硫酸常温制取氢气,并测定生成氢气的体积,他将从A-G中选择最佳的装置进行组合,整套装置的导管口连接顺序是b→c→d→h(填接口序号).
分析 长颈漏斗方便加液体药品,量筒可以测量一定体积的液体;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳和水反应生成碳酸,碳酸能使紫色变红色,加热时又变紫色;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳.在实验室用锌粒和稀硫酸常温制取氢气,因此不需要加热,因此选B;氢气难溶于水,因此可以用排水法收集,可以选用D;测定生成氢气的体积用G,他对装置进行组合是BDG,整套装置的导管口连接顺序是b→e→d→h;.
解答 解:(1)长颈漏斗方便加液体药品,量筒可以测量一定体积的液体,故答案为:长颈漏斗;量筒;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;若还想利用H装置收集一瓶干燥的氧气,则氧气应从短管进入,因为氧气的密度比空气大;故答案为:AF;固体需要加热制气体;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;m;
(3)二氧化碳和水反应生成碳酸,碳酸能使紫色变红色,加热时又变紫色;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;故答案为:CO2+H2O=H2CO3;红色又变紫色;CO2+Ca(OH)2=CaCO3↓+H2O;
(4)在实验室用锌粒和稀硫酸常温制取氢气,因此不需要加热,因此选B;氢气难溶于水,因此可以用排水法收集,可以选用D;测定生成氢气的体积用G,他对装置进行组合是BDG,整套装置的导管口连接顺序是b→e→d→h;故答案为:e→d→h;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的检验和性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 将足量的红磷和木炭分别放在如图所示的两个盛满空气的密闭集气瓶中燃烧,待燃烧停止并冷却后同时打开两装置的活塞,这时可观察到( )
将足量的红磷和木炭分别放在如图所示的两个盛满空气的密闭集气瓶中燃烧,待燃烧停止并冷却后同时打开两装置的活塞,这时可观察到( )| A. | 水先迅速进入A瓶 | B. | 水先迅速进入B瓶 | ||
| C. | 水迅速进入两个集气瓶中 | D. | 水不进入任何一个集气瓶中 |
| A. | 将金属钠保存在水中 | B. | 将盛有白磷和水的烧杯加热至60℃ | ||
| C. | 稀释浓硫酸 | D. | 用压强计测某一深度处的水压 |
| A. | 为加快过滤速度,用玻璃棒在漏斗中进行搅拌 | |
| B. | 过滤时,漏斗中液体的液面应低于滤纸边缘 | |
| C. | 蒸发时,有晶体析出后就不用玻璃棒搅拌 | |
| D. | 当蒸发皿中液体全部蒸干后,才能停止加热 |
| A. | 溶质的性质 | B. | 溶剂的性质 | C. | 温度 | D. | 搅拌 |
| A. | 酸雨就PH小于7的显酸性的雨水 | |
| B. | 合金的熔点要比组成它的纯金属的熔点高 | |
| C. | 在测定空气中氧气含量的实验中,红磷可以用木炭代替 | |
| D. | 除去硝酸钾溶液中的氯化钠,可以采用冷却热饱的溶液的方法 |
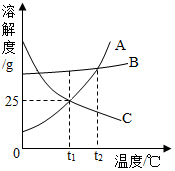 如图是A、B、C三种物质的溶解度曲线,下列说法正确的是( )
如图是A、B、C三种物质的溶解度曲线,下列说法正确的是( )| A. | 欲除去少量混在A中的B,提纯A物质可用蒸发结晶的方法 | |
| B. | t2℃时,等质量的B、C的饱和溶液中,溶剂的质量大小关系为B<C | |
| C. | t2℃时A、B、C的饱和溶液降温到t1℃时,A、C两溶液的溶质质量分数相等 | |
| D. | t1℃时,A的饱和溶液的溶质质量分数为25% |