题目内容
16.随着工农业发展,水资源的污染越来越严重,水资源的保护和合理利用已受到人们的普遍关注.(1)下列能确认水是由氢元素和氧元素组成的实验是A.
A.水的电解 B.水的蒸馏 C.海水淡化 D.水的蒸发
(2)某学校附近工长排出的废液中含有大量硫酸铜,对人体及农作物有害,若要测定废液的酸碱度,可选用pH试纸来测定,为帮助工厂治理废水并回收铜,可向废液中加入铁粉.
(3)水是常用的溶剂,若要配制100g15%的氯化钠溶液,配制时应选用100mL的量筒量取所需的水(填“10mL”“50mL”或“100mL”).
分析 (1)根据氢气的燃烧实验和水的电解实验都能证明水的元素组成解答;
(2)pH试纸可以测定溶液的酸碱度.要治理废水并且回收金属铜,应利用硫酸铜的化学性质即可作答;
(3)根据配制50g 5%的氯化钠溶液的步骤分析回答.
解答 解:
(1)A、水电解生成氢气和氧气,氢气是由氢元素组成的,氧气是由氧元素组成的,化学反应前后元素的种类不变,故说明水是由氢元素和氧元素组成的,故正确;
B、水的蒸馏是物理变化,无法证明水的元素组成,故错误;
C、海水淡化是物理变化,无法证明水的元素组成,故错误;
D、水的蒸发是物理变化,无法证明水的元素组成,故错误;
(2)若要测定废液的酸碱度,可选用pH试纸来测定.为帮助工厂治理废水并回收铜,可向废液中加入铁粉,铁粉能与之发生置换反应,置换出铜单质.然后过滤即可达到回收的目的.
(3)若要配制100g 15%的氯化钠溶液,需要进行如下的操作:需要氯化钠是:100g×15%=15g;水是:100g-15g=85g;合85mL
用100mL的量筒量取85mL水;
故答案为:(1)A;(2)pH试纸;铁粉;(3)100mL.
点评 此题以水资源的污染与防治为载体,考察了学生对硫酸铜的化学性质的掌握以及化学理论在生活生产中的实际应用.设计知识面广,基础性、能力性强.

练习册系列答案
相关题目
4.下列关于日常饮食习惯的说法正确的是( )
| A. | 火腿肠中添加有亚硝酸盐,应尽量少食用 | |
| B. | 碘、硒元素是人体必需的微量元素,应大量补充 | |
| C. | 过量摄入的油脂会使人发胖,应禁食油脂 | |
| D. | 蔬菜水果含有丰富的维生素,应代替米饭作为主食 |
11.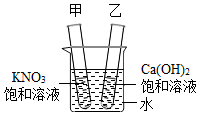 在如图所示的大烧杯中加入一定量的硝酸铵,溶解后甲试管内出现的现象以及乙试管内的溶液分别是( )
在如图所示的大烧杯中加入一定量的硝酸铵,溶解后甲试管内出现的现象以及乙试管内的溶液分别是( )
 在如图所示的大烧杯中加入一定量的硝酸铵,溶解后甲试管内出现的现象以及乙试管内的溶液分别是( )
在如图所示的大烧杯中加入一定量的硝酸铵,溶解后甲试管内出现的现象以及乙试管内的溶液分别是( )| A. | 无明显现象;不饱和溶液 | B. | 无明显现象;饱和溶液 | ||
| C. | 有晶体析出;不饱和溶液 | D. | 有晶体析出;饱和溶液 |
1.某化学兴趣小组将27.8g含杂质的纯碱样品(杂质为氯化钠)与181g稀盐酸相混合,充分反应,测得反应中生成气体的质量(m)与反应时间(t)的数据如表所示:
根据题目要求,回答下列问题:
(1)碳酸钠与稀盐酸反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O,碳酸钠完全反应后,生成CO2的质量为8.8g
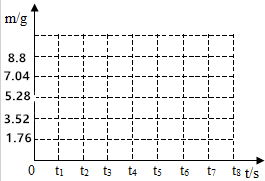
(2)请在如图所示的坐标图中,画出反应时生成气体的质量(m)随时间(t)变化的曲线.
(3)请计算完全反应后溶液中氯化钠的质量分数.
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 气体质量m/g | 0 | 1.76 | 3.52 | 5.28 | 7.04 | 8.8 | 8.8 |
(1)碳酸钠与稀盐酸反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O,碳酸钠完全反应后,生成CO2的质量为8.8g
(2)请在如图所示的坐标图中,画出反应时生成气体的质量(m)随时间(t)变化的曲线.

(3)请计算完全反应后溶液中氯化钠的质量分数.
8.以下物质的用途主要是由其化学性质决定的是( )
| A. | 干冰可用于冷藏食品 | B. | 氧气用于帮助呼吸 | ||
| C. | 活性炭用于除去冰箱中的异味 | D. | 石墨用于做电极 |
5.下列物质中含有氧分子的是( )
| A. | KMnO4 | B. | H2O2 | C. | CO2 | D. | 液态空气 |
 我在路边的围墙上看到一则化肥广告(如图):回校后,我通过计算氮的质量分数发现该广告是虚假广告.我认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现其氮元素质量分数仅为12.0%,我能算出该产品中碳酸氢铵的质量分数为67.8%.
我在路边的围墙上看到一则化肥广告(如图):回校后,我通过计算氮的质量分数发现该广告是虚假广告.我认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现其氮元素质量分数仅为12.0%,我能算出该产品中碳酸氢铵的质量分数为67.8%.