题目内容
9.美国科学家卡尔•克里斯特成功地制d得盐粒大小的氮5(化学式为N5),在制取氮5的实验中,它曾发生了爆炸,摧毁了实验室的部分设备,因此,科学家们认为,如果能让这种物质保持稳定;它可能会成为火箭和导弹后级的理想燃料.氮5是由排列成V形的5个氮原子结合而成的,化学性质极不稳定,需保存在-80℃的干冰中.根据以上叙述,你认为N5在应用领域有哪些用途?(写两条)(1)炸药;
(2)致冷剂.
分析 物质在化学变化中表现出来的性质叫化学性质,物质不需要发生化学变化就表现出来的性质,叫物理性质;物理性质经常表现为:颜色、状态、气味、密度、硬度、熔点、沸点、导电性、导热性、溶解性、挥发性等.由题目的信息可知,氮5是由排列成V形的5个氮原子结合而成的,化学性质极不稳定,需保存在-80℃的干冰中,因此N5的用途有:炸药、致冷剂、燃料等.
解答 解:由题目的信息可知,氮5是由排列成V形的5个氮原子结合而成的,化学性质极不稳定,需保存在-80℃的干冰中,因此N5的用途有:炸药、致冷剂、燃料等;故答案为:炸药;致冷剂;
点评 本考点考查了物质的性质和用途等,要根据题目给出的信息,并能够在比较的基础上进行应用,本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列有关宏观现象的微观解释中说法错误的是( )
| A. | 镁燃烧变成氧化镁时,镁原子的核电荷数发生了变化 | |
| B. | 氧气受热后体积变大,是因为分子受热后分子间间隔变大了 | |
| C. | 水电解生成氧气和氢气,是因为分子在化学变化中可以改变 | |
| D. | 未见饭菜就闻到饭菜的香味,说明分子在不停地运动 |
4.由NaHS、MgSO4、NaHSO3组成的混合物中,已知S元素的质量分数w(S)=a%,则O元素的质量分数w(O)为( )
| A. | 1.25a% | B. | 1.75a% | C. | 1-1.75a% | D. | 无法计算 |
14.向一定量的硫酸溶液中,分别加入足量的水、金属锌、氢氧化钠溶液、氯化钡溶液,下列图示正确的是( )
| A. | 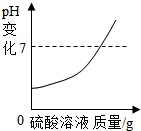 加足量水 | B. | 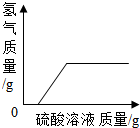 加足量锌 | ||
| C. | 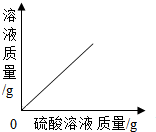 加足量NaOH溶液 | D. | 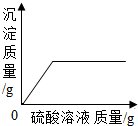 加足量BaCI2溶液 |
1.“塑化剂”是一种重要的化工原料,属2B类致癌物,曾被添加到食品中,造成了“塑化剂”风暴.已知“塑化剂”的化学式为C24H38O4.下列说法错误的是( )
| A. | 该“塑化剂”中碳、氢、氧三种元素的质量比为12:19:2 | |
| B. | 该“塑化剂”中碳的质量分数为73.8% | |
| C. | 该“塑化剂”属有机物 | |
| D. | 食品添加剂要严格按照国家规定标准进行使用 |
18.图片中不属于化学对人类贡献的是( )
| A. |  改良水稻品种 | B. |  合成药物 | C. |  合成新材料 | D. |  制作化学肥料 |
10. 已知氯化钠、碳酸钠在不同温度时的溶解度如表:
已知氯化钠、碳酸钠在不同温度时的溶解度如表:
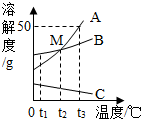
(1)依据上表,绘制了氯化钠和碳酸钠的溶解度曲线(如图),图中能表示碳酸钠溶解度曲线的是A(填“A”或“B”);
(2)图中两溶解度曲线相交于M点,此点表示的意义是t2℃时,A、B两物质的溶解度相等;
(3)40℃时,把50g A物质放入100g水中,充分搅拌,所得溶液是饱和(填“饱和”或“不饱和”)溶液;
(4)生活在盐湖(湖水中溶解有较多的氯化钠和碳酸钠)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”.请你答出“冬天捞碱”的道理:碳酸钠的溶解度受温度的影响较大,冬天温度较低,溶解在水中的碳酸钠会结晶析出.
 已知氯化钠、碳酸钠在不同温度时的溶解度如表:
已知氯化钠、碳酸钠在不同温度时的溶解度如表:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35 | 35.5 | 36 | 36.5 | 37 |
| 碳酸钠 | 6 | 10 | 18 | 36.5 | 50 | |
(2)图中两溶解度曲线相交于M点,此点表示的意义是t2℃时,A、B两物质的溶解度相等;
(3)40℃时,把50g A物质放入100g水中,充分搅拌,所得溶液是饱和(填“饱和”或“不饱和”)溶液;
(4)生活在盐湖(湖水中溶解有较多的氯化钠和碳酸钠)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”.请你答出“冬天捞碱”的道理:碳酸钠的溶解度受温度的影响较大,冬天温度较低,溶解在水中的碳酸钠会结晶析出.