��Ŀ����
��������������������������Ҫ��Դ��
��������⡿�����ǵ�ȼ�ղ�����CO2��H2O���ɴ��ܷ�֤����������ֻ��̼Ԫ�غ���Ԫ����ɵ��л��
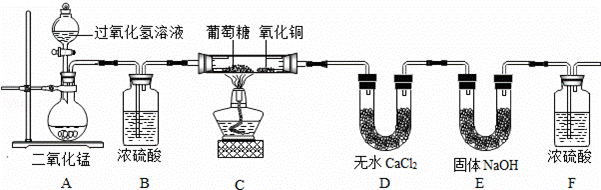
��ʵ����ơ�Ϊ��ȷ�������ǵ�Ԫ����ɣ�ijС�����������ʵ�飨����Ũ���ᡢ��ˮCaCl2��Ϊ���ø���������̶ֹ�װ��ʡ�ԣ���
��1��װ��A�з�����Ӧ�Ļ�ѧ����ʽ��������
��2��װ��C������ͭ������������
���������ۡ�
�ó��п����Ĵ��������װ��A���Ƿ��������ʵ��Ľ��У���������ǡ�����ԭ����������
�����ݴ������±���ͬѧ����д��ʵ�鱨�棬���������ɣ�
| ʵ����ʵ | ���ݷ��������� |
| 1.8g��������ȫȼ�գ��õ�2.64g CO2��1.08g H2O | ���ݷ��������� ���� ���ۣ������Ǻ���C��H��O����Ԫ�� |
| ʵ��̽�����ʵ���ɳɷ��Լ���������������ļ�������ӷ�����ʵ������ȡ�����ķ�Ӧԭ������������ijԪ�ص��������㣻�����غ㶨�ɼ���Ӧ�ã�. | |
| ר�⣺ | ѹ��ʵ���⣻��ѧ̽���� |
| ������ | ��ʵ����ơ���1�����ݹ�����������ʺͶ������̵Ĵ����ûش� ��2������һ����̼��������ͭ��Ӧ���ɱ������ɶ�����̼�����ʻش� ���������ۡ����ݿ�����Ҳ���ж�����̼�ش� �����ݴ��������������غ㶨�ɣ��������ǵ������������������������μӷ�Ӧ���������������ٸ��ݶ�����̼��ˮ�е���Ԫ�ص������������Ԫ�ص��������������������������Աȣ������������Ƿ�����Ԫ�أ� |
| ��� | �⣺��ʵ����ơ���1�����������ڶ������̵Ĵ���������Ѹ�ٷֽ�����������ˮ������ʽΪ2H2O2 ��2����ʵ����ⶨ��������̼Ԫ�ص�������ԭ���Ǹ��������������յĶ�����̼��������̼Ԫ�ص�������������ȼ��ʱ����Ҳ����һ����̼��Ϊ�˲ⶨ��ȷ��Ҫ�������Dz���ȫȼ�ղ���������CO������CO2������ͭͨ����һ����̼��Ӧ�ܱ�֤�������е�̼��ת��ΪCO2������������Dz���ȫȼ�ղ���������CO������CO2����֤�������е�̼��ת��ΪCO2�� ���������ۡ�������Ҳ���ж�����̼����Ӱ��������ȼ�����ɵĶ�����̼�����IJⶨ����������е�CO2�����ʵ�����IJⶨ�� �����ݴ��������������غ㶨�ɣ�������ȼ����O2��2.64g+1.08g��1.8g=1.92g����2.64gCO2����������Ϊ2.64g��32��44=1.92g��1.08gH2O����������Ϊ1.08g��16��18=0.96g�������������ܵ���Ԫ������Ϊ1.92g+0.96g=2.88g��2.88g��1.92g�����ԣ������Ǻ���C��H��O����Ԫ�أ� |
| ������ | ������һ���ۺ�ʵ���⣬��Ҫ����ѧ��������ѧ��ѧ֪ʶ�ۺϷ����ͽ��ʵ�������������������ѧ�����������˼ά��ȣ�ǿ����ѧ������֪ʶ�������� |
��

 �Ķ��쳵ϵ�д�
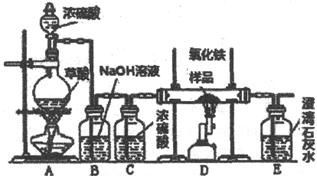
�Ķ��쳵ϵ�д�ijУ��ѧ������ȤС���ͬѧ���о���ѧϰ����չʾ��һ������ͼ��ʾ��ʵ��װ�ã�����ÿ����ѧ��Ӧ����ȫ����������Ʒ�е����ʲ��μӷ�Ӧ����
 |
 |
�������ϣ�������Ũ�������ʱ���ȷ������·�Ӧ��H2C2O4 CO��+CO2��+H2O��
ͨ�����ۣ�ͬѧ�Ƕ�����װ�����˶�����ʶ��
(1)Сǿͬѧ˵����ʵ�鰲ȫ�ǶȽ���ʵ�鿪ʼ�ȼ���___ _���A����D��������
ʵ�����ʱ��Ӧ____����ȡ���ֹͣD���ļ��ȣ��ӻ����ĽǶȽ�����Eװ��
��Ӧ��β�����д������䷽���ǣ�___ ��
(2 )С��ͬѧ˵���ø�ʵ��װ�ÿ��Լ���һ����̼����������Ӧ�����������Bװ��
)С��ͬѧ˵���ø�ʵ��װ�ÿ��Լ���һ����̼����������Ӧ�����������Bװ��
��������____ ������̼����������Ӧ�Ļ�ѧ����ʽ
Ϊ___ ��
(3)С��ͬѧ˵����������װ�û����Բⶨ��������Ʒ�����������������������ǵIJ�
�������ǣ�������������Ʒ������10 g����Ʒ�벣���ܵ�������Ϊ80 g����ȫ��Ӧ����ȴ��
�ٳ�����������ʣ������������Ϊ77.6g������ʵ������������Ʒ������������������
Ϊ____ ��
С��ͬѧѧϰ��ѧ�������е�һЩ��ʶ�������ܽᣬ���в��������ǣ�������
| �� | A�� | ���ɻ�Ƥ��ʱ��Ϊ���������������������ʵ�ɬζ���ɼ�������ʳ�� |
| �� | B�� | ����ú��ú��ȼ�ո���ȫ |
| �� | C�� | ʳ��ù��Ĵ��ס������Ȳ���Σ�����彡�� |
| �� | D�� | ��ȼ�յķ�������������ë�͵��� |
| �� | A�� | �Ȼ�淋��ܽ����� |
| �� | B�� | �����¶����ߣ������Ƶ��ܽ�Ȳ������� |
| �� | C�� | 40��ʱ�����Ʊ�����Һ���ʵ���������Ϊ50% |
| �� | D�� | ��40��ʱ��ͬ�����ı�����Һ���µ�20�棬����������������� |
ij�¶��£��� 3g A���ʷ���7gˮ�У��õ� 10g��Һ������Һ�ǣ�������
| �� | A�� | ������Һ | B�� | ��������Һ | C�� | Ũ��Һ | D�� | ��ȷ�� |
 2H2O+O2����
2H2O+O2���� �� ������������ ����������ϡ�����
�� ������������ ����������ϡ�����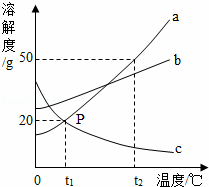
 ��200g����Ҫ������������Ϊ98%���ܶ�Ϊ1.84g��mL��1��Ũ��������Ϊ
��200g����Ҫ������������Ϊ98%���ܶ�Ϊ1.84g��mL��1��Ũ��������Ϊ