题目内容
20.生活中处处有化学,在实际生活中下列物质的用途只与其物理性质有关的是( )| A. | 二氧化碳做灭火剂 | |
| B. | 酒精用于给发烧病人擦拭以降低温度 | |
| C. | 氦气用作食品防腐剂 | |
| D. | 二氧化碳做温室的气体肥料 |
分析 物质的化学性质是指在化学变化中表现出来的性质,物质的物理性质是指不需要通过化学变化表现出来的性质,据此进行分析判断.
解答 解:A、二氧化碳做灭火剂,是利用了二氧化碳不燃烧、不支持燃烧和密度比空气大的性质,是利用了其化学性质和物理性质,故选项错误.
B、酒精用于给发烧病人擦拭以降低温度,是利用了酒精挥发吸热的性质,不需要发生化学变化就能表现出来,是利用了其物理性质,故选项正确.
C、氮气用作食品防腐剂,是利用了氮气化学性质稳定、无毒的性质,需要通过化学变化才表现出来,是利用了其化学性质,故选项错误.
D、二氧化碳做温室的气体肥料,是绿色植物利用了二氧化碳进行光合作用生成了新的物质,需要通过化学变化才表现出来,是利用了其化学性质,故选项错误.
故选B.
点评 本题难度不大,区分物质的用途是利用了物理性质还是化学性质,关键就是看利用的性质是否需要通过化学变化体现出来.

练习册系列答案
相关题目
8.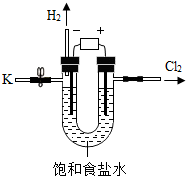 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
老师提示:
Ⅰ.电解饱和食盐水的化学方程式:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对本实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,确定待测液中含有氢氧化钠.
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入
一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
(2)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据计算所称取待测液中氢氧化钠的质量时,应选用稀盐酸的体积为9.8mL.
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁在溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
乙组同学按下图所示的实验步骤进行实验:
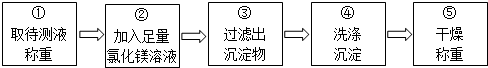
(3)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.
(4)步骤③过滤出的沉淀物是氢氧化镁.
(5)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.老师提示:
Ⅰ.电解饱和食盐水的化学方程式:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对本实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,确定待测液中含有氢氧化钠.
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入
一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁在溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
乙组同学按下图所示的实验步骤进行实验:

(3)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.
(4)步骤③过滤出的沉淀物是氢氧化镁.
(5)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
5.物质的结构决定物质的性质.下列关于物质的组成结构与性质的说法正确的是( )
| A. | 生铁和钢的性能不同,主要是由于其含碳量不同 | |
| B. | 水与过氧化氢的组成元素相同,化学性质也相同 | |
| C. | 金刚石和石墨的物理性质不同,是由于构成它们的碳原子不同 | |
| D. | 金属钠和镁的化学性质不同,主要是由于钠原子和镁原子的质子数不同 |
9.下列推测、推断或解释、归纳正确的是( )
| A. | 食盐溶液、蔗糖溶液是$\stackrel{推断}{→}$无色的液体都是溶液 | |
| B. | 在室温下的硝酸钾饱和溶液$\stackrel{推测}{→}$此时该溶液不能再溶解其它任何物质了 | |
| C. | 氢氧化钠溶于水时温度会升高$\stackrel{归纳}{→}$ 有些物质溶解时会吸热 | |
| D. | 向两张纸片之间吹气,纸片向中间靠拢 $\stackrel{解释}{→}$ 两纸片之间空气流速增大,导致气压比纸片外侧的大气压要小 |