题目内容
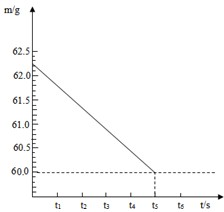 将碳酸钠和硫酸钠的固体混合物6g,放入烧杯中,再加入一定量的稀硫酸,在一定时间内恰好完全反应,无固体剩余,所得溶液溶质质量分数为19.5%,反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如右图所示:
将碳酸钠和硫酸钠的固体混合物6g,放入烧杯中,再加入一定量的稀硫酸,在一定时间内恰好完全反应,无固体剩余,所得溶液溶质质量分数为19.5%,反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如右图所示:(1)生成气体的质量为
(2)求所加稀硫酸的溶质质质量分数.
分析:(1)反应前后装置减少的质量为二氧化碳的质量.
(2)要求稀硫酸中溶质的质量分数,必须要知道硫酸的质量和稀硫酸的质量,硫酸的质量可根据二氧化碳的质量求出,稀硫酸的质量=反应所得溶液的质量+二氧化碳的质量-固体混合物的质量,二氧化碳和固体混合物的质量已知,反应所得溶液的质量=
,硫酸钠包括反应生成的硫酸钠和原混合物中的硫酸钠,反应生成的硫酸钠的质量可根据二氧化碳的质量求出,原混合物中的硫酸钠的质量=混合物的质量-碳酸钠的质量(可根据二氧化碳的质量求出).
(2)要求稀硫酸中溶质的质量分数,必须要知道硫酸的质量和稀硫酸的质量,硫酸的质量可根据二氧化碳的质量求出,稀硫酸的质量=反应所得溶液的质量+二氧化碳的质量-固体混合物的质量,二氧化碳和固体混合物的质量已知,反应所得溶液的质量=
| 硫酸钠的质量 |
| 19.5% |
解答:解:(1)二氧化碳的质量=62.2g-60g=2.2g
(2)设原混合物中碳酸钠的质量为x,参加反应的硫酸的质量为y,生成的硫酸钠的质量为z.
Na2CO3+H2SO4═Na2SO4+CO2↑+H2O
106 98 142 44
x y z 2.2g
=
,x=5.3g
=
,y=4.9g
=
,z=7.1g
反应所得溶液的质量=
=40g
稀硫酸的质量=40g+2.2g-6g=36.2g
则所加稀硫酸的溶质质量分数为:
×100%=13.5%
答:所加稀硫酸的溶质质量分数为13.5%.
(2)设原混合物中碳酸钠的质量为x,参加反应的硫酸的质量为y,生成的硫酸钠的质量为z.
Na2CO3+H2SO4═Na2SO4+CO2↑+H2O
106 98 142 44
x y z 2.2g
| 106 |
| x |
| 44 |
| 2.2g |
| 98 |
| y |
| 44 |
| 2.2g |
| 142 |
| z |
| 44 |
| 2.2g |
反应所得溶液的质量=
| 6 g -5.3g+7.1g |
| 19.5% |
稀硫酸的质量=40g+2.2g-6g=36.2g
则所加稀硫酸的溶质质量分数为:
| 4.9g |
| 36.2g |
答:所加稀硫酸的溶质质量分数为13.5%.
点评:本题是一道有关化学方程式和溶质质量分数的综合计算题,第一小题是最基本的根据质量守恒定律的计算;第二小题比较难,解题关键是要先求出反应后所得溶液的质量.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目



