题目内容
已知氯化钾(KCl)20℃时的溶解度是34 g,50℃时的溶解度是42.6g.通过如图的实验操作得到相应的溶液①~⑤.
20℃时100g水中
①
②
③
④
⑤
(1)上述各步实验所得溶液中,属于不饱和溶液的是 (填序号,下同);溶质的质量分数最大的是 ;溶液④的质量为 g.
(2)在50℃时,氯化钾的溶解度是42.6g,其含义是 .
20℃时100g水中
| 加入20gKCl |
| 加入20gKCl |
| 升温至50℃ |
| 加入20gKCl |
| 降温至20℃ |
(1)上述各步实验所得溶液中,属于不饱和溶液的是
(2)在50℃时,氯化钾的溶解度是42.6g,其含义是
考点:饱和溶液和不饱和溶液,固体溶解度的概念,溶质的质量分数
专题:溶液、浊液与溶解度
分析:根据固体的溶解度是指在一定温度下,某固体物质在100g水中达到饱和状态时所溶解的质量,根据固体物质的溶解度可以判断出在一定温度时形成的溶液是否饱和进行解答.
解答:解:由于氯化钾在20℃时的溶解度是34g,即100g水中最多溶解34g氯化钾,因此在20℃时在100g水中加入20g氯化钾,氯化钾会全部溶解,得到的①溶液是20℃不饱和溶液;又加入20g氯化钾,由于在100g水中最多溶解34g氯化钾,因此这20g氯化钾只能再溶解14g,所以形成的②溶液是20℃饱和溶液;升温至50℃,由于氯化钾在50℃时的溶解度是42.6g,因此后加入的氯化钾会全部溶解,而且形成的溶液③是50℃不饱和溶液,但又加入20g氯化钾,这20g氯化钾会再溶解2.6g,形成的溶液④是50℃饱和溶液,然后降温到20℃时,有晶体析出,形成溶液⑤是20℃饱和溶液.
(1)所得溶液中;为不饱和溶液的是①③;溶质的质量分数最大的是④,是50℃饱和溶液;溶液④的质量=100g+42.6g=142.6g;
(2)50℃时,氯化钾的溶解度是42.6g,其含义是50℃时,100g水中最多溶解42.6g氯化钾.
故答案为:(1)①③;④;142.6;
(2)50℃时,100g水中最多溶解42.6g氯化钾.
(1)所得溶液中;为不饱和溶液的是①③;溶质的质量分数最大的是④,是50℃饱和溶液;溶液④的质量=100g+42.6g=142.6g;
(2)50℃时,氯化钾的溶解度是42.6g,其含义是50℃时,100g水中最多溶解42.6g氯化钾.
故答案为:(1)①③;④;142.6;
(2)50℃时,100g水中最多溶解42.6g氯化钾.
点评:本题难度不大,主要考查了对固体溶解度概念的理解,从而培养学生对知识的应用能力和理解能力.

练习册系列答案
相关题目
下列实验基本操作不正确的是( )
A、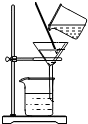 过滤 |
B、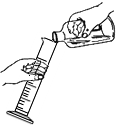 倾倒液体 |
C、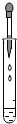 滴加液体药品 |
D、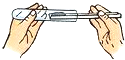 取用粉末状固体 取用粉末状固体 |
下列物质间的转换,不能一步实现的是( )
| A、Na2CO3→CaCO3 |
| B、H2O→O2 |
| C、KNO3→KCl |
| D、NaOH→NaCl |
下列实验现象描述正确的是( )
| A、把木条插入盛有氧气的集气瓶中,木条立即燃烧 |
| B、灼热的铁丝在氧气燃烧,火星四射,生成黑色固体,放出大量的热 |
| C、红磷在氧气中燃烧,产生浓厚的白雾 |
| D、硫在氧气中燃烧,发出明亮的蓝紫色火焰,产生浓厚的白烟 |
下列对实验现象的描述,正确的是( )
| A、铁丝在氧气中剧烈燃烧,火星四射,生成一种白色固体 |
| B、硫在氧气中燃烧发出微弱的淡蓝色火焰 |
| C、一氧化碳还原氧化铁的反应中,黑色粉末变成了红色 |
| D、磷在空气中燃烧放出大量白烟 |