题目内容
5.碳酸氢铵(化学式NH4HCO3)是农业生产中常用的铵态氮肥.(1)①碳酸氢铵中氮、氢、碳、氧四种元素的最简质量比为14:5:12:48;
②7.9 g碳酸氢铵中含4.8g氧元素.
(2)将15.8g碳酸氢铵加入到盛有100g稀盐酸的烧杯中,恰好完全反应.求反应后所得溶液的溶质质量分数.(写出计算步骤)
分析 (1)根据化学式计算对应元素质量比和求算某种元素的质量;
(2)根据碳酸氢钠的质量和对应化学方程式求算氯化铵和二氧化碳的质量,进而求算对应的氯化铵的质量分数.
解答 解:
(1)①碳酸氢铵(化学式NH4HCO3)中氮、氢、碳、氧四种元素的质量比为14:(1×5):12:(16×3)=14:5:12:48.
②含4.8g氧元素的碳酸氢铵的质量为4.8g÷($\frac{16×3}{14+1×5+12+16×3}$×100%)=7.9g.
(2)设15.8g碳酸氢铵完全反应生成的氯化铵的质量为x,生成的二氧化碳的质量为y
NH4HCO3+HCl═NH4Cl+H2O+CO2↑
79 53.5 44
15.8g x y
$\frac{79}{15.8g}$=$\frac{53.5}{x}$=$\frac{44}{y}$
x=10.7g
y=8.8g
反应后所得溶液的溶质质量分数为$\frac{10.7g}{15.8g+100g-4.4g}$×100%≈9.6%
答:(1)①碳酸氢铵中氮、氢、碳、氧四种元素的最简质量比为 14:5:12:48;
②7.9g碳酸氢铵中含4.8g氧元素.
(2)将15.8g碳酸氢铵加入到盛有100g稀盐酸的烧杯中,恰好完全反应.求反应后所得溶液的溶质质量分数为9.6%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
15.分类是学习化学的方法之一,下列各组物质是按单质,氧化物,混合物进行分类的是( )
| A. | 液氧 熟石灰 空气 | |
| B. | 活性炭 酒精 碘盐 | |
| C. | 生铁 干冰 矿泉水 | |
| D. | 金刚石 冰 高锰酸钾制氧气的剩余固体 |
16.下列物质中属于纯净物的是( )
| A. | 加碘食盐 | B. | 烧碱 | C. | 矿泉水 | D. | 浓硫酸 |
13.下列有关水的净化和处理,说法正确的是( )
| A. | 生活污水应集中处理,达标后再排放 | |
| B. | 过滤能除去水中所有的杂质 | |
| C. | 硬水经活性炭吸附后变成软水 | |
| D. | 电解水生成氢气和氧气的质量比约为2:1 |
17.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | CO2和SO2都能和NaOH溶液反应,CO也能和NaOH溶液反应 | |
| B. | CO和C都能和CuO反应生成Cu,有还原性,H2也能和CuO反应生成Cu,也有还原性 | |
| C. | 活泼金属和盐酸反应生成气体,和盐酸反应生成气体的物质是活泼金属 | |
| D. | 氢氧化钙和氢氧化钠都属于碱,都含有金属元素,所以碱都含有金属元素 |
14.下列相关实验方法能达到目的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 鉴别稀硫酸和硫酸钠溶液 | 滴加酚酞 |
| B | 鉴别氢气和甲烷 | 点燃,火焰上罩一个冷而干燥的烧杯 |
| C | 除去KCl固体中的MnO2 | 溶解、过滤和蒸发 |
| D | 除去NaCl溶液中少量的Na2CO3 | 加入足量的石灰水,过滤 |
| A. | A | B. | B | C. | C | D. | D |
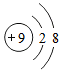 是某微粒的结构示意图,其符号为F-;
是某微粒的结构示意图,其符号为F-;