题目内容
3.硅是太阳能电池和电脑芯片不可缺少的材料.利用石英砂(主要成分为二氧化硅)生产高纯硅的流程图如图(整个制备过程必须达到无水、无氧气).请回答: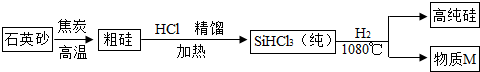
(1)二氧化硅中硅元素的化合价是+4.
(2)该流程中无氧气的原因可能是防止氢气与氧气混合高温时发生爆炸,同时防止硅被氧化.
(3)以上流程中,可循环使用的物质是HCl.
分析 (1)根据在化合物中正负化合价代数和为零,进行分析解答.
(2)根据生产高纯硅的流程图,过程中使用了氢气,氢气具有可燃性,与氧气混合在加热时易发生爆炸,且硅在高温条件下能与氧气反应生成二氧化硅,进行分析解答.
(3)根据既是反应物,也是生成物的物质,可以循环使用进行分析解答.
解答 解:(1)氧元素显-2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
(2)由生产高纯硅的流程图,过程中使用了氢气,氢气具有可燃性,与氧气混合在加热时易发生爆炸,且硅在高温条件下能与氧气反应生成二氧化硅,故该流程中无氧气的原因可能是防止发生爆炸,防止硅被氧化.
(3)氢气与SiHCl3反应生成高纯硅和M(由质量守恒定律,反应前后元素种类不变,则该物质为氯化氢),既是反应物,也是生成物的物质可以循环使用,则生产过程中可循环使用的物质是HCl.
故答案为:(1)+4;(2)防止氢气与氧气混合高温时发生爆炸,同时防止硅被氧化;(3)HCl.
点评 本题难度不大,理解生产高纯硅的流程图,掌握化合物中正负化合价代数和为零、防止爆炸的措施等是正确解答本题的关键.

练习册系列答案
相关题目
13.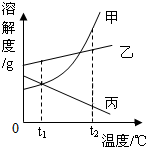 如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )
如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )
 如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )
如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )| A. | 三种物质溶解度大小依次为:乙>丙>甲 | |
| B. | 将温度由t2℃降到t1℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>丙>甲 | |
| C. | 若甲中含有少量杂质乙,不能用降温结晶的方法进行提纯 | |
| D. | 将温度由t2℃降到t1℃时,析出甲的质量比乙多 |
14.逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
| A. | 因为酸性的溶液能使石蕊变红,所以酸溶液一定能使石蕊变红 | |
| B. | 因为酸和碱中和反应生成盐和水,所以生成盐和水一定是中和反应 | |
| C. | 因为金属能和酸反应产生氢气,所以能和酸产生气体的一定是金属 | |
| D. | 因为H2O和H2O2的组成元素相同,所以它们的化学性质相同 |
6.下列对实验现象的描述正确的是( )
| A. | 红磷燃烧产生大量的白色烟雾,放出热量 | |
| B. | 电解水时电极两端有气泡生成,并且正极与负极产生氧气和氢气的体积比约为1:2 | |
| C. | 硫在氧气中燃烧,产生蓝紫色火焰,放热,生成有刺激性气味的气体 | |
| D. | 碳在氧气中燃烧更旺,发出白色火焰 |