题目内容
17.如图是实验室常用的一些装置,请根据问题回答:
(1)实验室用高锰酸钾制取氧气的文字表达式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,若用装置D收集氧气,验满的方法是把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
(2)实验室使用过氧化氢溶液和二氧化锰制取氧气的文字表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,最好选用图中的C做发生装置,你认为选用此装置的优点是能够控制反应速率.
(3)欲使用装置E用排水法收集氧气,则先将E装满水,再将气体从b(填a或b)端通入.
(4)已知实验室可以用重铬酸铵固体加热后制取氮气,则选用图中的A做发生装置.氮气的密度约等于空气的密度,且不溶于水,因此氮气可选用图中的F做收集装置.
分析 (1)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
氧气的密度比空气的密度大,不易溶于水,能够支持燃烧,能使带火星的木条复燃;
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
注射器能够控制液体药品的流量,从而能够控制反应速率;
(3)根据装置的特点,可以判断气体的进出方向;
(4)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
解答 解:(1)实验室用高锰酸钾制取氧气的文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
若用装置D收集氧气,验满的方法是:把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
故填:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
(2)实验室使用过氧化氢溶液和二氧化锰制取氧气的文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
因为反应不需要加热,C中的注射器能够控制反应速率,因此最好选用图中的C做发生装置.
故填:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;C;能够控制反应速率.
(3)欲使用装置E用排水法收集氧气,则先将E装满水,再将气体从b端通入.
故填:b.
(4)实验室用重铬酸铵固体制取氮气需要加热,则选用图中的A做发生装置;
氮气的密度约等于空气的密度,不能用排空气法收集,不溶于水,可以用排水法收集,即用F装置收集.
故填:A;F.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
8.下列物质长时间放置在敞口的容器中,溶液质量会增加但不会变质的是( )
| A. | NaOH | B. | 浓HCl | C. | 浓H2SO4 | D. | 石灰水 |
12.下列有关实验现象描述正确的是( )
| A. | 红磷在空气中燃烧,产生大量的白雾 | |
| B. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色的四氧化三铁 | |
| C. | 木炭在氧气中燃烧,发出白色火焰,生成使澄清石灰水变浑浊的气体 | |
| D. | 镁在空气中燃烧,发出耀眼的白光,放出大量热,生成白色固体 |
9.了解安全知识,可以更好地保护人身和财产安全.下列做法不正确的是( )
| A. | 发现燃气泄漏应立即开窗通风关阀门 | |
| B. | 霉变的大米、瓜子、花生等不能食用 | |
| C. | 用甲醛溶液浸泡水产品 | |
| D. | 室内起火应压低身体逃离火场 |
6.生活中发生的下列变化,属于化学变化的是( )
| A. | 玻璃破碎 | B. | 冰块融化 | C. | 粮食酿酒 | D. | 汽油挥发 |
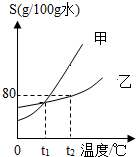 如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:
如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题: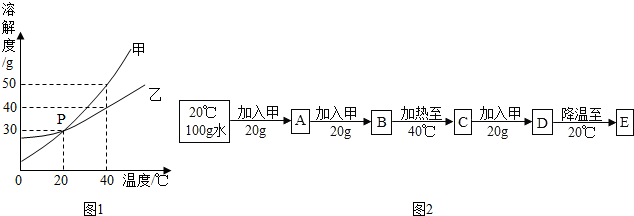


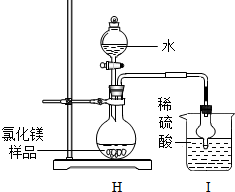
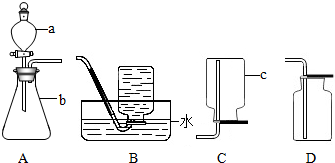 实验室部分装置如图所示,请回答下列问题:
实验室部分装置如图所示,请回答下列问题: