题目内容
14.实验课上,同学们学习了氧气和二氧化碳的实验室制法,他们对气体的制法进行了总结,并利用如图所示装置进行练习和拓展.请回答下列问题: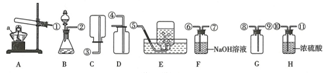
(1)知识总结
【反应原理】
实验室用高锰酸钾制氧气的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
用大理石制二氧化碳的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.
【气体制备】
用高锰酸钾制氧气的发生装置是A,制二氧化碳的发生装置是B(填字母序号,下同).
【气体制备】
实验室收集O2的装置是D、E或G,收集CO2的装置是D或G.
【实验步骤及注意事项】
实验室用高锰酸钾制取氧气主要的实验步骤有,①加热②装药品并固定试管③检查装置的气密性④用排水法收集氧气⑤停止加热⑥将导管从水槽中取出,正确的操作顺序是③②①④⑥⑤.
A装置中试管口略向下倾斜的目的是防止冷凝水倒流,炸裂试管,用排水法收集氧气,开始收集的适宜时刻是气泡连续均匀冒出时.
【气体验满】
检验CO2是否收集满的方法是将燃烧的木条放在集气瓶口,看是否熄灭
【气体检验】
检验瓶中气体是否为O2的方法是将带火星的木条伸入集气瓶内,看是否复燃.
(2)知识应用
现有如下资料:
①制取NO2的反应原理:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
②通常状况下,NO2是一种密度比空气大的有毒气体,能与水发生反应.
③NO2能与碱溶液反应生成盐和水.
知识拓展
在实验室中,集气瓶被称做“万能瓶”,用它可以组装成各种用途的装置,请仔细观察下列各个装置的特点回答问题:
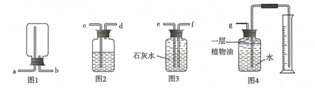
(1)实验室若用图1装置收集氧气,则氧气应从b(填导管口符号)口进入.
(2)实验室若用图2装置干燥氧气,则瓶中的液体为浓硫酸,则氧气应从c(填导管口符号)口进入.
(3)若要收集一定体积的二氧化碳气体,应选用图4装置.
(4)若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯净的一氧化碳,应选用图3装置.
分析 (1)【反应原理】根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
【气体制备】根据实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,实验室制取二氧化碳的反应物是固体和液体,反应条件是常温进行分析;
【气体制备】根据氧气密度比空气大,不易溶于水,二氧化碳密度比空气大,易溶于水进行分析;
【实验步骤及注意事项】根据实验室用高锰酸钾制取氧气的正确步骤,以及实验的正确操作进行分析;
【气体验满】根据二氧化碳不具有助燃性进行分析;
【气体验满】根据氧气有助燃性进行分析;
(2)1)根据氧气密度比空气大进行分析;
2)根据浓硫酸有吸水性,洗气时,应该长进短出进行分析;
3)根据二氧化碳易溶于水进行分析;
4)根据二氧化碳会与氢氧化钙反应生成碳酸钙沉淀和水进行分析.
解答 解:(1)【反应原理】高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
【气体制备】实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以发生装置是:A;
实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以发生装置是:B;
【气体制备】氧气密度比空气大,不易溶于水,所以实验室收集O2的装置是:D、E或G;
二氧化碳密度比空气大,易溶于水,所以收集CO2的装置是:D或G;
【实验步骤及注意事项】实验室用高锰酸钾制取氧气需要先组装仪器,然后检验装置气密性,装药,制取气体,收集,实验结束先撤导管,后熄灭酒精灯,所以正确的操作顺序是:③②①④⑥⑤;
A装置中试管口略向下倾斜的目的是:防止冷凝水倒流,炸裂试管,用排水法收集氧气,开始收集的适宜时刻是:气泡连续均匀冒出时;
【气体验满】二氧化碳不具有助燃性,所以验满的方法是:将燃烧的木条放在集气瓶口,看是否熄灭;
【气体验满】氧气有助燃性,所以检验瓶中气体是否为O2的方法是:将带火星的木条伸入集气瓶内,看是否复燃;
(2)1)氧气密度比空气大,所以实验室若用图1装置收集氧气,则氧气应从b口进入;
2)浓硫酸有吸水性,洗气时,应该长进短出,所以实验室若用图2装置干燥氧气,则瓶中的液体为浓硫酸,则氧气应从c口进入;
3)二氧化碳易溶于水,所以若要收集一定体积的二氧化碳气体,应选用图4装置;
4)二氧化碳会与氢氧化钙反应生成碳酸钙沉淀和水,所以若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯净的一氧化碳,应选用图3装置.
故答案为:(1)【反应原理】2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;CaCO3+2HCl=CaCl2+H2O+CO2↑;
【气体制备】A;B;
【气体制备】D、E或G;D或G;
【实验步骤及注意事项】③②①④⑥⑤;防止冷凝水倒流,炸裂试管;气泡连续均匀冒出时;
【气体验满】将燃烧的木条放在集气瓶口,看是否熄灭;
【气体验满】将带火星的木条伸入集气瓶内,看是否复燃;
(2)1)b;
2)浓硫酸,c;
3)图4;
4)图3.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 名校课堂系列答案
名校课堂系列答案| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①③④ |
| A. | 红磷在氧气中剧烈燃烧,生成大量白色烟雾 | |
| B. | 硫在空气中燃烧,发出蓝紫色火焰,生成白烟 | |
| C. | 煤炭在空气中燃烧,生成二氧化碳气体 | |
| D. | 生石灰与水反应,放出热量 |
 已知铁丝在氧气中可以燃烧,反应时剧烈燃烧,火星四射,生成黑色固体,试回答:
已知铁丝在氧气中可以燃烧,反应时剧烈燃烧,火星四射,生成黑色固体,试回答: