题目内容
16.CO和CO2的混合气体10g与足量灼热的氧化铜反应后,测得质量比原来增加4g,则原混合气体中CO和CO2的质量比为7:3.分析 此题根据“跟踪氧原子的去向”来解决问题.二氧化碳不能与氧化铜反应,一氧化碳与氧化铜反应生成二氧化碳和铜.CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2反应后气体的质量比原来增加了32%,增加的质量就是反应的氧化铜中氧原子的质量,用差量法得出氧的质量,然后根据一氧化碳的相对分子质量与一氧化碳的质量比等于氧的相对原子质量与氧的质量比,列出比例式,就可求出混合气体中一氧化碳的质量,进而计算出二氧化碳的质量,然后比较即可.
解答 解:设混合气体中一氧化碳的质量为x,
CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2----O
28 16
x 4g
∴$\frac{28}{16}=\frac{x}{4g}$,∴x=7g;
则混合气体中二氧化碳的质量为:10g-7g=3g;
则原混合气体中CO、CO2的质量比为:7g:3g=7:3.
故答案为:7:3.
点评 本题主要考查学生运用差量法和化学方程式进行计算的能力.题目中的条件隐蔽,需要认真分析数量关系,才能正确解答.

练习册系列答案
相关题目
4.两包粉末,一是铁粉,二是氧化铜粉,快速将它们鉴别出来的方法是( )
| A. | 观察颜色,加以鉴别? | |
| B. | 分别加水溶解,加以鉴别? | |
| C. | 用磁铁吸引,加以鉴别 | |
| D. | 装入试管中分别加热,再分别通入H2观察现象,加以鉴别? |
11.纳米材料被誉为21世纪最有前途的新型材料,许多材料达到纳米(1纳米=10-9米)级的大小时,会产生许多让你料想不到的、奇特的光、电、磁、热、力和化学等方面的性质.如:将金属制成纳米粉末后就变成了黑色,且不导电,机械强度也大幅度提高.由此你判断下列说法错误的是( )
| A. | 纳米碳质地很柔软,构成其的基本粒子是碳原子 | |
| B. | 纳米氧化锌能吸收电磁波 | |
| C. | 黑色的氧化铜粉末属于纳米材料 | |
| D. | 若将银白色铁通过特殊加工成纳米粉末,其物理性质将发生一定的变化 |
5.下表是小华对自己吸人的气体和呼出的气体进行探究的结果:
①请你判断x是氮气,y是氧气.
②请你回答:
因参与新陈代谢而被人体消耗的是氧气.
③请你证明:
呼出气体中含有较多水蒸气,你们实验方法是:对着干燥而冷却的玻璃片呼气,玻璃片上出现较多的水雾,说明呼出气体中含有较多的水蒸气.
| 气体 | x | Y | 二氧化碳 | 水蒸气 |
| 吸入气体 | 78.26% | 21.04% | 0.03% | 0.67% |
| 呼出气体 | 74.88% | 15.26% | 3.68% | 6.18% |
②请你回答:
因参与新陈代谢而被人体消耗的是氧气.
③请你证明:
呼出气体中含有较多水蒸气,你们实验方法是:对着干燥而冷却的玻璃片呼气,玻璃片上出现较多的水雾,说明呼出气体中含有较多的水蒸气.
6.下列实验操作,正确的有几项( )
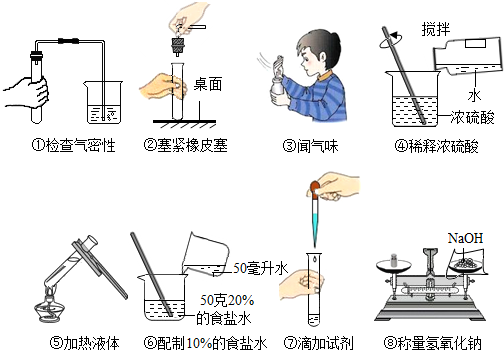

| A. | 3项 | B. | 4项 | C. | 5项 | D. | 6项 |
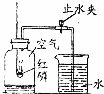 用如图所示装置进行″探究空气中氧气含量″的实验.实验步骤如下:①先用止水夹夹紧橡皮管;②点燃燃烧匙里的红磷;③迅速将燃烧匙插入集气瓶,并塞紧塞子;④燃烧完毕并冷却后,打开止水夹.
用如图所示装置进行″探究空气中氧气含量″的实验.实验步骤如下:①先用止水夹夹紧橡皮管;②点燃燃烧匙里的红磷;③迅速将燃烧匙插入集气瓶,并塞紧塞子;④燃烧完毕并冷却后,打开止水夹.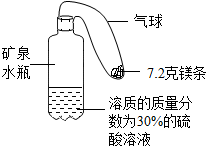 某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).将气球中的镁条加入到硫酸溶液中,恰好完全反应.
某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).将气球中的镁条加入到硫酸溶液中,恰好完全反应. ;⑦纯碱不是碱而是盐Na2CO3.
;⑦纯碱不是碱而是盐Na2CO3.