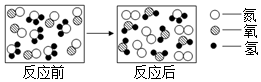
题目内容
12.如表所示实验方案正确的是B| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去硫酸铁溶液中的硫酸铜 | 加入足量的铁粉,过滤 |
| B | 硬水软化 | 煮沸或蒸馏 |
| C | 检验露置于空气中的氢氧化钠溶液是否变质 | 滴入无色酚酞 |
| D | 鉴别氯化钠和硝酸铵固体 | 加水(或加熟石灰研磨) |
分析 A、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
B、根据硬水软化的方法,进行分析判断.
C、根据变质后的氢氧化钠溶液中含有碳酸钠,进行分析判断.
D、根据两种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们.
解答 解:A、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所示实验方案正确.
B、用煮沸或蒸馏的方法可以硬水软化,故选项所示实验方案正确.
C、变质后的氢氧化钠溶液中含有碳酸钠,碳酸钠、氢氧化钠均显碱性,均能使无色酚酞变红色,不能证明氢氧化钠溶液是否已变质,故选项所示实验方案正确.
D、硝酸铵溶于水吸热,使溶液的温度降低,氯化钠溶于水温度几乎无变化,可以鉴别(或加熟石灰研磨).
故答案为:B;加水(或加熟石灰研磨).
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体解题时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
2.化学小组的同学探究二氧化碳和氢氧化钠的反应,实验方案如下:•
(1)步骤①中气球鼓起的原因可能是NaOH溶液吸收了CO2,导致瓶内压强减小.
(2)步骤②中的操作是向外拉注射器3,其目的是证明步骤1中将瓶内的CO2全部吸收了.
(3)步骤①中发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
(4)本实验的结论是CO2能和NaOH发生反应.
| 实验装置 | 实验步骤及操作 | 实验现象 |
 | ①将注射器1中的溶液推入充有CO2的瓶中 | 气球鼓起 |
| ②向外拉注射器3 | 无明显现象 | |
| ③将注射器2中的溶液推入瓶中 | 溶液中有气泡产生,气球变瘪 | |
| ④向外拉注射器3 | 澄清石灰水变浑浊 |
(2)步骤②中的操作是向外拉注射器3,其目的是证明步骤1中将瓶内的CO2全部吸收了.
(3)步骤①中发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
(4)本实验的结论是CO2能和NaOH发生反应.
4.给试管中的液体加热时,若出现试管破裂的现象,其原因不可能是( )
| A. | 加热前试管外壁有水 | B. | 加热不均匀,局部温度过高 | ||
| C. | 试管内的液体超过 $\frac{1}{3}$ | D. | 试管触及灯芯了 |
1.20℃时,A物质的溶解度为15g,40℃时,A物质的溶解度为30g.试分析上述状态下属于饱和溶液的是( )


| A. | ③④⑤⑥ | B. | ③④⑥ | C. | ③⑤⑥ | D. | ③⑥ |
2.小科同学为测定某含铁混合物中的含铁量,做了如下实验:称取11.4g样品,放入质量为50.0g的烧杯中,再往烧杯内加入足量的100.0g稀盐酸(杂质不与酸反应、不溶于水),并对烧杯进行了四次称量,记录的数据如下.求:
(1)反应产生的氢气质量;
(2)该混合物中铁的质量分数.
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯总质量/g | 161.4 | 161.2 | 161.0 | 161.0 |
(2)该混合物中铁的质量分数.
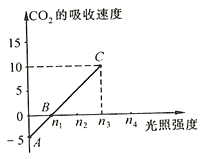 植物的新陈代谢要受到外界环境因素(如光、水分)的影响.如图表示一株叶面积为10分米2的植物在一定光照和一定二氧化碳浓度的条件下吸收二氧化碳的速度(单位:毫克/(分米2•小时)).请回答:
植物的新陈代谢要受到外界环境因素(如光、水分)的影响.如图表示一株叶面积为10分米2的植物在一定光照和一定二氧化碳浓度的条件下吸收二氧化碳的速度(单位:毫克/(分米2•小时)).请回答: