��Ŀ����
13��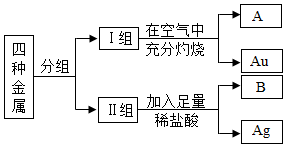 ij����С���ͬѧ����ʦ�İ����´ӷ����ҵ��л��������Fe����ͭ��Cu��������Ag������Au�����ֽ�����������������ֽ����أ�ͬѧ�ǽ�������ʵ�飺
ij����С���ͬѧ����ʦ�İ����´ӷ����ҵ��л��������Fe����ͭ��Cu��������Ag������Au�����ֽ�����������������ֽ����أ�ͬѧ�ǽ�������ʵ�飺��1��ͬѧ�Ǿ����۲�ܿ콫���ֽ�����Ϊ���飮���ǵķ�����������ɫ��ͬ��
��2��A�ڿ��������յ��������ɺ�ɫ��ɺ�ɫ��B��ϡ���ᷴӦ�Ļ�ѧ����ʽΪFe+2HCl�TFeCl2+H2����
��3���������������ֽ�����ͬʱ����������֤�������˳���ɢ�����Ի�֪�Ļ��˳�������������ã���Ҫ��֤Cu��Ag�Ļ��˳���貹��һ��ʵ�飬д��ʵ�����ܷ�����Ӧ�Ļ�ѧ����ʽCu+2AgNO3=Cu��NO3��2+2Ag��
��4�����շ������������Ӳ�Ʒ�еĽ������ϼȿ��Լ��ٻ�����Ⱦ���ֿ��Ա���������Դ������������Դ��;�����к�������������Դ��дһ�����ɣ���
���� ��1�����Ǻ�ɫ���壬ͭ�Ǻ�ɫ���壬��������ɫ���壬���ǻ�ɫ���壻
��2��ͭ�ڿ���������ʱ���ܺ����е�������Ӧ���ɺ�ɫ��������ͭ�����ܺ�ϡ���ᷴӦ�����Ȼ�������������
��3�����ܺ�ϡ���ᷴӦ�������ܺ�ϡ���ᷴӦ��
ͭ�������ã��ܺ���������Ӧ��������ͭ������
��4������������Դ��;�����У��������÷Ͼɽ�������������������Դ��Ѱ�ҽ�����Դ�����Ʒ�ȣ�
��� �⣺��1�����Ǻ�ɫ���壬ͭ�Ǻ�ɫ���壬��������ɫ���壬���ǻ�ɫ���壬������ǵķ�����������ɫ��ͬ��
�����ɫ��ͬ��
��2��A��ͭ���ڿ���������ʱ���ܺ����е�������Ӧ���ɺ�ɫ��������ͭ������ڿ��������յ��������ɺ�ɫ��ɺ�ɫ��
B��������ϡ���ᷴӦ�����Ȼ���������������Ӧ�Ļ�ѧ����ʽΪ��Fe+2HCl�TFeCl2+H2����
����ɺ�ɫ��ɺ�ɫ��Fe+2HCl�TFeCl2+H2����
��3���ɢ�����Ի�֪�����ܺ�ϡ���ᷴӦ�������ܺ�ϡ���ᷴӦ��˵�����������ã�
��Ҫ��֤Cu��Ag�Ļ��˳���貹����һ��ʵ���ǣ���ͭ˿������������Һ�У�ͭ˿���渽��һ������ɫ���壬˵��ͭ�������ã�ͭ����������Ӧ��������ͭ��������Ӧ�Ļ�ѧ����ʽΪ��Cu+2AgNO3=Cu��NO3��2+2Ag��
������������ã�Cu+2AgNO3=Cu��NO3��2+2Ag��
��4�����շ������������Ӳ�Ʒ�еĽ������ϼȿ��Լ��ٻ�����Ⱦ���ֿ��Ա���������Դ������������Դ��;�����У���������������Դ��Ѱ�ҽ�����Դ�����Ʒ�ȣ�
�����������������Դ��
���� Ҫ�����ý����˳�������ʵ�飬��ǰ�ߵĽ�������ϡ���ᡢ���ᷴӦ�������ߵĽ���������ϡ���ᡢ���ᷴӦ��ǰ�ߵĽ�����Ѻ�ߵĽ�����������Һ���û�������

| A�� | ѹǿ���������ܽ�Ȳ��� | B�� | �¶����������ܽ�ȼ�С | ||
| C�� | ѹǿ��С�������ܽ������ | D�� | �¶Ƚ��������ܽ�ȼ�С |
 Ϊ����ij������ͭ��ͭ��ɵĻ����������ͭ����������ȡ3�ݸû�����20g���ֱ������뵽50g��100g��150gijϡ�����У��������ʵ���������±���
Ϊ����ij������ͭ��ͭ��ɵĻ����������ͭ����������ȡ3�ݸû�����20g���ֱ������뵽50g��100g��150gijϡ�����У��������ʵ���������±���| ��� | A | B | C |
| ϡ���������/g | 50 | 100 | 150 |
| ʣ����������/g | 10.0 | 16.0 | 16.0 |
��1��ʵ���з�Ӧ������ͭ��ʣ�����A�飮
��2��20g�û������Ʒ�к�����ͭ������Ϊ16g��
��3������A�����ݼ������õ�ϡ�������ʵ�����������д��������̣�
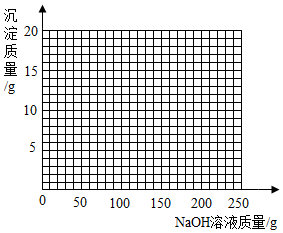
��4����B��������ˣ�����Һ�еμ�10%��NaOH��Һ�������ڸû����Һ�м���10%NaOH��Һ�����������ɳ��������仯��ϵ������ͼ��
��ʾ������Һ�����ʺ���H2SO4��CuSO4����Ӧ���Ⱥ�˳�����£�
H2SO4+2NaOH=2H2O+Na2SO4
CuSO4+2NaOH=Cu��OH��2��+Na2SO4��
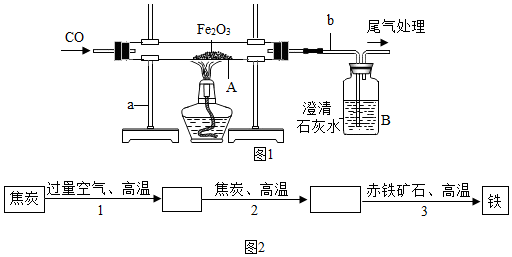

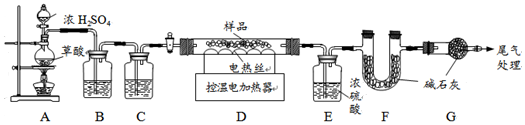

 Ϊ�ⶨijBaCl2��Һ����������������ȡ100g��BaCl2��Һ�����ϼ���ϡH2SO4����Ӧ��������Һ���������ϡH2SO4��������ϵ��ͼ��ʾ��
Ϊ�ⶨijBaCl2��Һ����������������ȡ100g��BaCl2��Һ�����ϼ���ϡH2SO4����Ӧ��������Һ���������ϡH2SO4��������ϵ��ͼ��ʾ��