题目内容
18.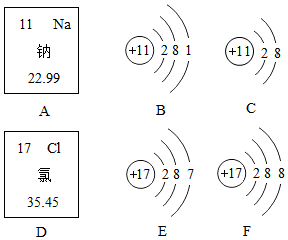 根据如图所示钠元素和氯元素的相关信息,回答下列问题:
根据如图所示钠元素和氯元素的相关信息,回答下列问题:(1)A中的11是钠元素的质子数;
(2)氯元素的相对原子质量是35.45;
(3)钠元素和氯元素形成的氯化钠中,阴阳离子的个数比是1:1;
(4)B、C、E、F中,能确定钠元素和氯元素所处周期的是BE.
分析 (1)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,结合原子结构示意图的信息进行分析判断即可;
(2)根据图中元素周期表可以获得的信息解答;
(3)根据氯化钠的结构来分析;
(4)根据周期数等于原子核外的电子层数来分析.
解答 解:
(1)由元素周期表的信息可知,钠的原子序数为11,原子序数=质子数,所以质子数为11;
(2)根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为35.45.
(3)由钠原子结构示意图为可以看出:最外层弧线上的数字是1,原子最外电子层上有1个电子,在化学反应中易失去1个电子而形成阳离子.
氯原子的最外层电子数为7,大于4个,易得到1个电子,转化成氯离子,钠元素和氯元素形成的氯化钠中,阴阳离子的个数比是1:1;
(4)周期数等于原子核外的电子层数,B中质子数=核外电子数,是钠原子=11,E中质子数=核外电子数=17,是氯原子
钠原子和氯原子核外均为3个电子层,故均位于第三周期,
答案:(1)质子; (2)35.45; (3)1:1; (4)BE.
点评 本题的难度不大,了解原子结构示意图的意义和元素周期表中一个格的含义是解答本题的基础知识.

练习册系列答案
相关题目
9.下列化学方程式与对应反应类型均正确的是( )
| A. | Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O+CO2↑ 分解反应 | |
| B. | 4Al+3O2=2A12O3 化合反应 | |
| C. | 2Fe+6HC1=2FeCl3+3H2↑ 置换反应 | |
| D. | CO2+2NaOH═Na2CO3+H2O 复分解反应 |
6.葡萄糖(C6H12O6),乙酸(CH3COOH)和甲醛(CH2O)组成的混合物240g,在一定条件下完全燃烧,生成水的质量为( )
| A. | 48g | B. | 72g | C. | 120g | D. | 144g |
13.下列化学用语与表示的意义不相符的是( )
| A. | Al2O3:氧化铝 | B. | $\stackrel{+2}{Mg}$:镁离子 | ||
| C. | 2H2O:两个水分子 | D. | $\stackrel{0}{O}$2:氧气中氧元素的化合价为零 |
14.在实验室中,配制质量分数为10%的NaOH溶液,用于制作“叶脉书签”,下列说法正确的是( )
| A. | 将NaOH固体直接放在托盘上称量 | |
| B. | NaOH有强烈的腐蚀性,实验时最好戴防护眼镜 | |
| C. | 溶解时玻璃棒的作用是搅拌,增大NaOH的溶解度 | |
| D. | 若在量取水时俯视凹液面的最低处,则配制溶液的质量分数小于10% |
15.下列实验基本操作正确的是( )
| A. |  | B. | 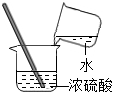 | C. | 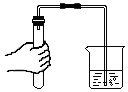 | D. | 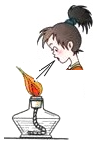 |
 .
.