��Ŀ����
6������ͬѧ�ڻ�ѧʵ�������������ʵ�飬ȡһ������þ�ۼӵ��ձ��м���һ������ϡ���ᣬ�ټ�������������Һ���˺������к����������| ��һ�� | �ڶ��� | |
| þ�� | m | m |
| ϡ���� | 50g | 100g |
| ����������Һ | 100g | 100g |
| ������ù��� | 4.1g | 5.8g |
| ʵ������ | �� | ��ɫ���� |
��1��д��ʵ��������巴Ӧ�Ļ�ѧ���ʽMg+H2SO4=MgSO4+H2����
��2����-��ʵ���Ĺ������ʳɷּ�����þ��������þ���õ���ɫ����
��3�����ݵڶ������ɹ����������ⷴӦ���������������ı���ʽ$\frac{80}{x}$=$\frac{58}{5.8g}$��
��4��m��������2.4g
��5������ڶ���ʵ������Һ�м���3.6gˮ�������õ���Һ�����ʵ���������7.1%��
���� ��1������þ�����ᷴӦ��������þ���������з�����
��2����������þ���������Ʒ�Ӧ����������þ�����������ƽ��з�����
��3�����ݵڶ������ɵĹ�����������þ���������ݻ�ѧ����ʽ���м��㣻
��4������þԪ���غ���м��㣻
��5��������Һ����������������������������������
��� �⣺��1��þ�����ᷴӦ��������þ����������ѧ����ʽΪ��Mg+H2SO4=MgSO4+H2����
��2������þ�����ᷴӦ��������þ������������þ���������Ʒ�Ӧ����������þ�����������ƣ��Ա�����ʵ������ݿ�֪����һ�μ�������ᣬþû����ȫ��Ӧ�����Ե�һ��ʵ���Ĺ������ʳɷ���þ��������þ��ʵ�������ǵõ���ɫ���壻
��3����μӷ�Ӧ��������������Ϊx����������������Ϊz
MgSO4+2NaOH=Mg��OH��2��+Na2SO4
80 58 142
x 5.8g z
$\frac{80}{x}$=$\frac{58}{5.8g}$=$\frac{142}{z}$
z=14.2g
��3����m������Ϊy
����Mg+H2SO4=MgSO4+H2����MgSO4+2NaOH=Mg��OH��2��+Na2SO4����֪
Mg----Mg��OH��2��
24 58
y 5.8g
$\frac{24}{y}$=$\frac{58}{5.8g}$
y=2.4g
���ݻ�ѧ����ʽ��֪��2.4��þ��������0.2g��������
��5���������õ���Һ�����ʵ���������Ϊ��$\frac{14.2g}{2.4g+100+100g-0.2g-5.8g+3.6g}$��100%=7.1%��
�ʴ�Ϊ����1��Mg+H2SO4=MgSO4+H2����
��2��þ��������þ���õ���ɫ���壻
��3��$\frac{80}{x}$=$\frac{58}{5.8g}$
��3��2.4g
��5��7.1%��
���� ������Ҫ�����˻�ѧ����ʽ�ļ��㣬�ѶȽϴ�ע�����Ĺ淶�Ժ�ȷ�ԣ�

| A�� | ��˿��� | B�� | ����ȼ�� | C�� | �������� | D�� | ���ɺ�ɫ���� |
| A�� | ˮ | B�� | ���� | C�� | ��� | D�� | �Ȼ��� |
| A�� |  �ⶨ�����������ĺ��� �ⶨ�����������ĺ��� | |
| B�� |  ���ȸ������������ ���ȸ������������ | |
| C�� |  �õ���������Ũ�ȵ�˫��ˮ�ֱ���ȡ���� �õ���������Ũ�ȵ�˫��ˮ�ֱ���ȡ���� | |
| D�� | 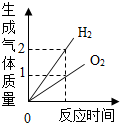 ���ˮ ���ˮ |
 ��֪A��B��C��D��E��F��Ϊ���л�ѧ�г��������ʣ��ҳ�E����������ж����еؿ��к�������Ԫ�أ�����A��C��Ϊ��ɫҺ�������Ԫ����ͬ��BΪ��ɫ���壬���ǵ�ת����ϵ��ͼ��ʾ�����ַ�Ӧ������ʡ�ԣ���
��֪A��B��C��D��E��F��Ϊ���л�ѧ�г��������ʣ��ҳ�E����������ж����еؿ��к�������Ԫ�أ�����A��C��Ϊ��ɫҺ�������Ԫ����ͬ��BΪ��ɫ���壬���ǵ�ת����ϵ��ͼ��ʾ�����ַ�Ӧ������ʡ�ԣ���