题目内容
2.“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气.实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量.【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【查阅资料】
①2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2═2Na2CO3+O2
②碳酸钠溶液显碱性,氯化钙溶液显中性.
【猜想与假设】
(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是Na2O2和Na2CO3的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
…
【设计实施方案】
| 实验步骤 | 实验现象 |
| ①取3.00g变质粉末于一支大试管内,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体. | 固体完全溶解,带火星木条复燃, 不用填 |
| ②继续向上述试管中加入足量的石灰水,充分反应. | 有白色沉淀生成 |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g. |
粉末中含有的成分及质量
| Na2O2 | NaOH | Na2CO3 | |
| 成分(填“有”或“没有”) | |||
| 质量(g) |
(1)实验室在保存过氧化钠时应注意密封保存.
(2)有同学提出把第②步实验中足量的石灰水改为足量氯化钙溶液,至沉淀不再生成时过滤,向滤液中滴加无色酚酞试液,若液体变红,则证明原粉末中有NaOH.你认为该方案是否合理并说明理由不合理,因为过氧化钠与水反应能生成氢氧化钠,不能判断原来是否存在氢氧化钠..
分析 【猜想与假设】根据过氧化钠与水反应,与二氧化碳反应的生成物考虑可能猜想;
【设计与方案】根据气体的检验方法可知是氧气,根据将②中物质过滤,得到滤渣推测是否含有碳酸钙进而推出实验现象;
【解释与结论】根据生成氧气质量计算出过氧化钠的质量,根据生成碳酸钙沉淀的质量计算出碳酸钠的质量,用总质量减去过氧化钠质量,再减去碳酸钠的质量就是氢氧化钠的质量;
【反思与评价】根据过氧化钠易与二氧化碳和水反应推出保存方法;根据过氧化钠与水反应能生成氢氧化钠,可推出结论是否正确.
解答 解:【猜想与假设】Na2O2与二氧化碳反应生成Na2CO3和氧气,所以固体可能是碳酸钠和过氧化钠的混合物;
【设计与方案】检验气体用的是带火星的木条,所以是氧气,氧气能使带火星的木条复燃;根据将②中物质过滤,得到滤渣可知有白色沉淀生成;
【解释与结论】设要生成0.32g氧气需过氧化钠的质量为x,则:
2Na2O2+2H2O═4NaOH+O2↑
156 32
x 0.32g
$\frac{156}{x}$=$\frac{32}{0.32g}$
x=1.56g,所以含过氧化钠质量为1.56g;
设要生成1.00g碳酸钙沉淀需要碳酸钠的质量为y,则;
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100
y 1.00g
$\frac{106}{y}$=$\frac{100}{1g}$
y=1.06g,
所以混合物中含有氢氧化钠质量为:3g-1.56g-1.06g=0.38g;
【反思与评价】
(1)过氧化钠易与二氧化碳反应,还能和水反应变质所以要密封保存;
(2)向滤液中滴加无色酚酞试液,若液体变红,不能证明原粉末中有NaOH,因为过氧化钠与水反应能生成氢氧化钠,不能说明原来是否存在.
故答案为:【猜想与假设】(2)Na2O2 和Na2CO3;
【设计实施方案】
| 实验操作 | 实验现象 |
| 固体完全溶解,有气泡产生,带火星木条复燃. | |
| 产生白色沉淀 |
| Na2O2 | NaOH | Na2CO3 | |
| 成分(填“有”或“没有”) | 有 | 有 | 有 |
| 质量(g) | 1.56 | 0.38 | 1.06 |
(2)不合理,因为过氧化钠与水反应也能生成氢氧化钠,也能使无色酚酞试液变红,所以不能证明原粉末中有NaOH.
点评 解答本题的关键是要知道收集到0.32g气体是氧气质量,将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g属于碳酸钙的质量.

| A. |  一定质量的溶液稀释时加入水质量与溶质质量的变化 | |
| B. |  t1℃时,A、B两物质的饱和溶液的溶质质量相等 | |
| C. | 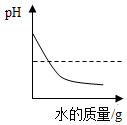 向NaOH溶液中加盐酸时,溶液PH的变化 | |
| D. | 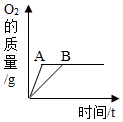 用AB两份等质量等浓度的双氧水制取氧气,A中加入了二氧化锰 |
| A. | 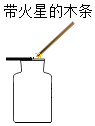 验满氧气 验满氧气 | B. |  称量氢氧化钠固体 称量氢氧化钠固体 | ||
| C. |  测定溶液的pH 测定溶液的pH | D. |  |
 |  | 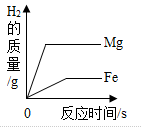 | 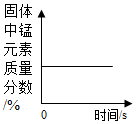 |
| A、向一定量稀盐 酸中加水稀释 | B、向硫酸和硫酸铜的混合稀溶液中,逐滴加入氢氧化钠溶液 | C、足量的镁片和铁片分别与等质量、等质量分数稀盐酸反应 | D、加热一定量的 高锰酸钾固体 |
| A. | A | B. | B | C. | C | D. | D |
| 实验序号 | 反应物的质量/g | 产物的质量/g | |
| X | Y | ||
| ① | 7.2 | 1.6 | 8.0 |
| ② | 8.0 | 2.4 | 10.0 |
| A. | 18.0g | B. | 18.8g | C. | 19.0g | D. | 19.2g |
| A. | 患佝偻病 | B. | 引起贫血 | C. | 产生龋齿 | D. | 骨质疏松 |
| A. | 具有均一性、稳定性的液体一定是溶液 | |
| B. | 配制溶液时,搅拌可以增大固体溶质的溶解度 | |
| C. | 饱和溶液的浓度一定比不饱和溶液的浓度大 | |
| D. | 配制氢氧化钠溶液时,必须将氢氧化钠固体放在玻璃器皿中称量 |