题目内容
4.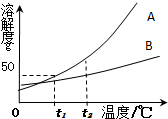 A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题
A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题(1)t1℃时,A的饱和溶液中溶质与溶液质量比1:3
(2)若B中含有少量A,应用蒸发结晶法提纯B;
(3)若将A的饱和溶液从t2℃降温到t1℃时,一定不会发生改
变的是B.
A.溶解度 B.溶剂质量 C.溶质质量 D.溶质质量分数
(4)粗盐提纯实验中,已知20℃时NaCl的溶解度为36g,本实验溶解3.6g的粗盐,蒸馏水的最佳使用量约为10ml.增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是水太多,过滤的时间太长;不利于后续蒸发溶剂,蒸发溶剂时间会大大延长,消耗燃料.
分析 根据题目信息和溶解度曲线可知:A、B两种固体物质的溶解度,都是随温度升高而增大,而A的溶解度随温度的升高变化比B大;t1℃时,A的饱和溶液中溶质与溶液质量比=50g:150g=1:3;若B中含有少量A,应用蒸发结晶法提纯B,因为B的溶解度受温度的影响不大;若将A的饱和溶液从t2℃降温到t1℃时,一定不会发生改
变的是溶剂质量;粗盐提纯实验中,已知20℃时NaCl的溶解度为36g,本实验溶解3.6g的粗盐,蒸馏水的最佳使用量约为10ml;增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是水太多,过滤的时间太长;不利于后续蒸发溶剂,蒸发溶剂时间会大大延长,消耗燃料.
解答 解:(1)t1℃时,A的饱和溶液中溶质与溶液质量比=50g:150g=1:3;故答案为:1:3;
(2)若B中含有少量A,应用蒸发结晶法提纯B,因为B的溶解度受温度的影响不大,故答案为:蒸发结晶;
(3)若将A的饱和溶液从t2℃降温到t1℃时,一定不会发生改变的是溶剂质量;故答案为:B;
(4)看图2可知,20℃时NaCl的溶解度为36g,本实验溶解3.6g的粗盐,蒸馏水的最佳使用量约为10g,因为水的密度是1.0g/mL,因此是10mL;增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是水太多,过滤的时间太长;不利于后续蒸发溶剂,蒸发溶剂时间会大大延长,消耗燃料;故答案为:10;水太多,过滤的时间太长;不利于后续蒸发溶剂,蒸发溶剂时间会大大延长,消耗燃料;
点评 本考点考查了溶解度曲线及其应用、结晶的方法等,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
14.下列关于碳及其氧化物的说法中,正确的是( )
| A. | 一氧化碳和二氧化碳都可以将氧化铜还原为铜 | |
| B. | 二氧化碳的排放不是导致酸雨的原因 | |
| C. | 在室内放一盆澄清石灰水可防止一氧化碳中毒 | |
| D. | 铅笔字迹易变模糊是因为常温下石墨化学性质活泼 |
15.下列变化中不属于缓慢氧化的是( )
| A. | 动植物呼吸 | B. | 食物腐败 | C. | 酒精燃烧 | D. | 铁制品锈蚀 |
19.下列认识或说法中正确的是( )
| A. | 铝的化学性质稳定,可在铁栏杆的表面涂铝粉防止生锈 | |
| B. | 用pH试纸测得某地水的pH为5.2 | |
| C. | 配制溶液时,如俯视量筒读数则会导致质量分数偏大 | |
| D. | 某单质X能从某溶液中置换出Y,X是金属时,Y可能是金属,也可能是非金属 |
16.在一定的条件下,向一密闭的容器内加入A、B、C、D四种物质各20g,充分反应后,测定其质量,得到数据如下:
下列说法不正确的是( )
| 物质 | A | B | C | D |
| 反应前质量(g) | 20 | 20 | 20 | 20 |
| 反应后质量(g) | 20 | 30 | 未知 | 14 |
| A. | A物质可能是该反应的催化剂 | B. | 容器内发生了化合反应 | ||
| C. | 反应后容器内C的质量为16g | D. | 其化学方程式为:2C+3D═5B |
13.下列做法与“创建文明城市,建设生态洪泽”不吻合的是( )
| A. | 植树种草 | B. | 就地焚烧垃圾 | ||
| C. | 节能减排 | D. | 公共场所禁止吸烟 |
14.香烟燃烧产生的烟气中含有许多强致癌物和有害物质,其中对人体危害最大的是尼古丁(化学式C10H14N2)、焦油和一氧化碳等.下列说法中错误的是( )
| A. | 学校应当成为无烟场所 | |
| B. | 尼古丁由碳、氢和氮三种元素组成 | |
| C. | C10H14N2中,碳、氢、氮三种元素的质量比为10:14:2 | |
| D. | CO易与血液里的血红蛋白结合,使血红蛋白携氧能力降低 |