题目内容
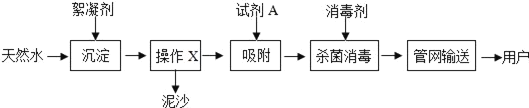
某电镀厂为减少污染及节约成本,从含有硫酸铜、硫酸锌、硫酸亚铁的废水中回收重要原料硫酸锌和有有关金属,实验过程如图:

①步骤 I、IV 包含的相同操作是_____。
②写出步骤 I 中反应的化学方程式_____。
③上述步骤_____(选填步骤编号)所包含的反应体现了锌的活动性比铜强。
④要计算废液中硫酸铜质量,必须要称量_____的质量。(实验过程中的物质损失忽略不计)
⑤判断步骤 IV 中加入的稀硫酸足量的方法是_____。
练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
下列除去杂质所选用的方法正确的是( )
选项 | 物质 | 杂质 | 除杂方法 |
A | O2 | CO2 | 点燃 |
B | Cu(OH)2固体 | NaOH固体 | 加足量水搅拌,过滤,洗涤,干燥 |
C | NaOH溶液 | Na2CO3 | 加入过量稀盐酸 |
D | 银粉 | 锌粉 | 加入过量硫酸亚铁溶液 |
A. A B. B C. C D. D
某同学对若干块矿石样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应).请计算:
序号 | 加入稀盐酸质量(g) | 剩余固体质量(g) |
第1次 | 10 | 5.5 |
第2次 | 10 | m |
第3次 | 10 | 1.2 |
第4次 | 10 | 1.2 |
(1)8g的石灰石样品中含有杂质_____克?
(2)如表中m的数值应为_____?
(3)稀盐酸的质量分数是多少?_____