题目内容
1.元素周期表中部分元素的相关信息如下,回答下列问题: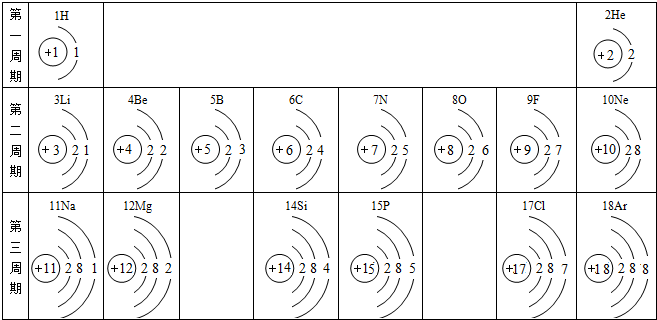 (1)12号元素的原子形成的离子是Mg2+(写离子符号),16号元素的原子最外层电子数为6,地壳中含量最多的金属元素和非金属元素组成的化合物是Al2O3(写化学式).
(1)12号元素的原子形成的离子是Mg2+(写离子符号),16号元素的原子最外层电子数为6,地壳中含量最多的金属元素和非金属元素组成的化合物是Al2O3(写化学式).(2)金属元素的原子在化学反应中易失去电子(选填“得”或“失”),稀有气体元素的原子不易得失电子.
(3)在元素周期表中,同一族的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是ACD
A.He和Ar B. He和Mg C.Li和Na D.F和Cl.
分析 (1)根据最外层电子数来确定得失电子情况并书写符号进行解答;根据最外层电子数相同化学性质相似进行解答;根据地壳中元素的含量写化学式;
(2)根据最外层电子数来确定得失电子的情况;
(3)根据最外层电子数决定化学性质解答.
解答 解:(1)12号元素是镁元素,根据镁原子结构示意图可知,其最外层有2个电子,在化学反应中易失去最外层的2个电子而带两个单位的正电荷;形成的粒子的符号Mg2+;它的核外电子排布与氖元素的原子核外电子排布相同;16号元素是硫元素.其原子最外层电子数为6;地壳中含量最多的金属元素是铝和非金属元素是氧,二者组成的化合物是 Al2O3;
(2)金属原子的最外层电子数一般少于4个,在反应中容易失去电子而满足最外层8电子的稳定结构;
(3)最外层电子数相同则化学性质相似,故具有相似化学性质的是①He和Ar,④F和Cl;
故答案为:(1)Mg2+ 6 Al2O3 (2)失 (3)ACD
点评 本题考查元素的原子结构以及特点,掌握原子在化学反应中得失电子的规律是解题的关键所在.

练习册系列答案
相关题目
9.“归纳与比较”是学习化学的重要方法,某同学对C、H2、CO三种物质的“归纳与比较”有:①构成:都由分子构成;②性质:都具有可燃性和还原性;③用途:都可以用来冶炼金属; ④状态:常温下都为气态.其中均正确的是( )
| A. | ②③ | B. | ①② | C. | ①③ | D. | ②④ |
16.下列属于化学变化的是( )
| A. | 酒精挥发 | B. | 风力发电 | C. | 干冰升华 | D. | 牛奶变酸 |
13. 向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是C.
向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是C.
 向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是C.
向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是C.| 烧杯中的物质 | X溶液 | |
| A | 稀硫酸和稀盐酸 | 氯化钡溶液 |
| B | 澄清石灰水 | 碳酸钠溶液 |
| C | 稀硫酸光和硫酸铜溶液 | 氢氧化钠溶液 |
| D | 碳酸钠和氢氧化钠溶液 | 稀盐酸 |
10.化学知识的整理和归纳对于化学的学习非常重要,以下是某同学对所学的化学知识进行归纳和推理,其中正确的是( )
| A. | 酸的溶液pH<7,碱的溶液pH>7,但是盐的溶液pH不一定等于7 | |
| B. | 氧化物中含有氧元素,所以含有氧元素的化合物就是氧化物 | |
| C. | 碳酸盐与稀盐酸反应产生气体,所以与稀盐酸反应产生气体的物质一定是碳酸盐 | |
| D. | 二氧化碳的大量排放会增强地球的温室效应,所以二氧化碳是空气污染物 |
11.下列生活用品,其中用金属材料制作而成的是( )
| A. | 陶瓷杯 | B. | 不锈钢碗 | C. | 塑料盆 | D. | 玻璃茶壶 |
