题目内容
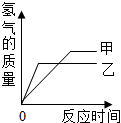 现有等质量的甲、乙两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与时间的关系如图(已知甲、乙在生成物中的化合价均为+2价).则下列说法不正确的是( )
现有等质量的甲、乙两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与时间的关系如图(已知甲、乙在生成物中的化合价均为+2价).则下列说法不正确的是( )| A、生成氢气的质量:甲>乙 |
| B、相对原子质量:乙>甲 |
| C、金属活动性甲>乙 |
| D、消耗硫酸的质量:甲>乙 |
考点:金属的化学性质
专题:金属与金属材料
分析:A、根据图象分析生成氢气的质量;
B、根据甲、乙在生成物中化合价均为+2价,可知等质量的金属与足量的稀硫酸完全反应,产生氢气的质量与金属的相对原子质量成反比分析;
C、据相同时间内产生氢气较多(即反应剧烈)的金属活动性较强,结合产生氢气的关系图判断两种金属活动性;
D、根据质量守恒定律定律可知,生成氢气的质量取决于消耗的硫酸的质量.
B、根据甲、乙在生成物中化合价均为+2价,可知等质量的金属与足量的稀硫酸完全反应,产生氢气的质量与金属的相对原子质量成反比分析;
C、据相同时间内产生氢气较多(即反应剧烈)的金属活动性较强,结合产生氢气的关系图判断两种金属活动性;
D、根据质量守恒定律定律可知,生成氢气的质量取决于消耗的硫酸的质量.
解答:解:
A、根据反应生成H2的质量与反应时间的关系图所示,在两种金属完全反应后,放出H2的质量是甲>乙,正确;
B、根据甲、乙金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在金属完全反应后,放出H2的质量是甲>乙,因此可判断相对原子质量是乙>甲,故说法正确;
C、根据反应生成H2的质量与反应时间的关系图所示,相同时间内乙放出氢气的质量大于甲,可判断金属活动性顺序是乙>甲,故说法错误;
D、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:甲>乙,故说法正确;
故选:C.
A、根据反应生成H2的质量与反应时间的关系图所示,在两种金属完全反应后,放出H2的质量是甲>乙,正确;
B、根据甲、乙金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在金属完全反应后,放出H2的质量是甲>乙,因此可判断相对原子质量是乙>甲,故说法正确;
C、根据反应生成H2的质量与反应时间的关系图所示,相同时间内乙放出氢气的质量大于甲,可判断金属活动性顺序是乙>甲,故说法错误;
D、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:甲>乙,故说法正确;
故选:C.
点评:活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比,据此结合图象细心分析解答.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
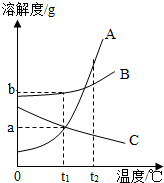 如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.下列有关说法错误的是( )
如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.下列有关说法错误的是( )| A、t1℃三种物质中B物质的溶解度大 |
| B、t2℃三种物质的饱和溶液中,溶质的质量分数最大的是A |
| C、可用升高温度的方法使t1℃时C的饱和溶液变为不饱和溶液 |
| D、A中混有少量C时,可用降温结晶法分离提纯 |
下列说法中正确的是( )
| A、酸的溶液显酸性,所以显酸性的溶液一定是酸的溶液 |
| B、离子是带电的原子或原子团,所以带电的微粒一定是离子 |
| C、碱的溶液显碱性,但显碱性溶液不一定是碱溶液 |
| D、向某物质中加入稀盐酸产生无色无味气体,则该物质中一定含有碳酸根离子或碳酸氢根离子 |
金属Mn分别放入两种金属X、Y的盐溶液中,充分反应后有无金属析出如下表所示.
它们的金属活动性由强到弱的顺序为( )
| X的盐溶液 | Y的盐溶液 | |
| Mn | 无 | 有 |
| A、X>Mn>Y |
| B、Y>Mn>X |
| C、Mn>Y>X |
| D、X>Mn>Y |
有人利用摄影店废弃的定影液回收银.一种回收方法的反应原理是:Fe+2AgNO3═2Ag+Fe(NO3)2这个反应属于( )
| A、化合反应 | B、分解反应 |
| C、置换反应 | D、无法确定 |
下列符号表示正确的是( )
| A、2个氢分子:2H | ||
| B、4个氧原子:2O2 | ||
C、氧化铝中铝元素的化合价:
| ||
| D、3个硝酸根离子:3NO3- |
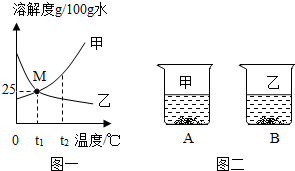 图一为甲、乙两种物质(不带结晶水)的溶解度曲线图.
图一为甲、乙两种物质(不带结晶水)的溶解度曲线图.