题目内容
探究二氧化碳溶于水时,是否与水发生了化学反应?实验方案:取四朵用石蕊试液染成紫色的干燥小花,按下图中的步骤I~Ⅳ依次进行实验,观察小花的颜色变化 (资料:紫色石蕊试液遇酸变红色).
I.纸花变红Ⅱ.纸花不变红Ⅲ.瓶中的纸花不变红Ⅳ.纸花变红
(1)由步骤 可以得出结论:使石蕊变红的是醋酸不是水:
(2)步骤Ⅲ的作用是 .
(3)通过上述哪些实验步骤 ,可以证明二氧化碳与水发生反应,写出二氧化碳溶于水时发生反应的化学方程式 .

I.纸花变红Ⅱ.纸花不变红Ⅲ.瓶中的纸花不变红Ⅳ.纸花变红
(1)由步骤
(2)步骤Ⅲ的作用是
(3)通过上述哪些实验步骤

考点:探究二氧化碳的性质,书写化学方程式、文字表达式、电离方程式
专题:碳单质与含碳化合物的性质与用途
分析:依据石蕊遇酸性溶液会变红以及二氧化碳溶于水会生成碳酸等知识结合各对比实验的情况分析解决即可.
解答:解:(1)I.纸花变红Ⅱ.纸花不变红,说明使石蕊变红的是醋酸不是水.
步骤III中存在二氧化碳气体,二氧化碳不具备酸性所以纸花不会变红,步骤IV中纸花喷水后放入盛有二氧化碳的集气瓶,则水与二氧化碳会生成碳酸,碳酸会使石蕊变红,所以纸花变红.
(2)步骤III中只存在二氧化碳气体,因为二氧化碳不具备酸性所以纸花不会变红,证明二氧化碳不能使石蕊变红,
(3)步骤Ⅱ说明:水不能使石蕊变红;步骤Ⅲ说明:二氧化碳不能使石蕊变红;步骤IV中纸花喷水后放入盛有二氧化碳的集气瓶,则水与二氧化碳会生成碳酸,碳酸会使石蕊变红,所以纸花变红,能证明碳酸能使石蕊变红.
该实验中发生了二氧化碳与水的反应,产物是碳酸,其方程式为:CO2+H2O═H2CO3;
故答案为:(1)Ⅰ、Ⅱ(2)二氧化碳不能使石蕊变红;(3)Ⅱ、Ⅲ、Ⅳ;CO2+H2O═H2CO3
步骤III中存在二氧化碳气体,二氧化碳不具备酸性所以纸花不会变红,步骤IV中纸花喷水后放入盛有二氧化碳的集气瓶,则水与二氧化碳会生成碳酸,碳酸会使石蕊变红,所以纸花变红.
(2)步骤III中只存在二氧化碳气体,因为二氧化碳不具备酸性所以纸花不会变红,证明二氧化碳不能使石蕊变红,
(3)步骤Ⅱ说明:水不能使石蕊变红;步骤Ⅲ说明:二氧化碳不能使石蕊变红;步骤IV中纸花喷水后放入盛有二氧化碳的集气瓶,则水与二氧化碳会生成碳酸,碳酸会使石蕊变红,所以纸花变红,能证明碳酸能使石蕊变红.
该实验中发生了二氧化碳与水的反应,产物是碳酸,其方程式为:CO2+H2O═H2CO3;
故答案为:(1)Ⅰ、Ⅱ(2)二氧化碳不能使石蕊变红;(3)Ⅱ、Ⅲ、Ⅳ;CO2+H2O═H2CO3
点评:此题考查了石蕊的特点以及二氧化碳与水的反应,解题的关键是分清各对比实验的目的以及相关的化学反应,属于常规实验考查题.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
下列实验现象的描述正确的是( )
| A、硫在氧气里燃烧,发出蓝紫色火焰 |
| B、红磷燃烧产生大量白雾 |
| C、碳在氧气里燃烧,发出蓝色火焰,生成黑色固体 |
| D、铁丝在氧气中燃烧,火星四射,生成白色固体 |
下列实验方案能达到实验目的是( )
| A | B | C | D | |
| 方案 |  |  |  |  |
| 目的 | 证明二氧化碳溶于水且能和水反应 | 证明碳与氧化铜能发生反应 | 证明金属锌的活动性比铁的活动性强 | 证明燃烧的条件是温度需达到可燃物的着火点 |
| A、A | B、B | C、C | D、D |
自来水生产时,向水中通氯气,这是因为氯气跟水反应,生成了盐酸和次氯酸,其中次氯酸具有强氧化性,可起到灭菌作用,某学生用自来水配制下列溶液,通常不会使药品明细变质的是( )
| A、食盐水 | B、硝酸银溶液 |
| C、石蕊试液 | D、碳酸钠溶液 |
下列有关碳和碳的化合物的说法不正确的是( )
| A、一氧化碳具有还原性可用于冶炼金属 |
| B、金刚石、石墨、C60完全燃烧都生成CO2 |
| C、室内放一盆水能防止一氧化碳中毒 |
| D、可用澄清石灰水鉴别CO2和CO两种气体 |

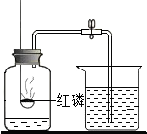 在一次实验课上同学们组装了如图装置进行实验:
在一次实验课上同学们组装了如图装置进行实验: