题目内容
【题目】某化学制剂厂甲、乙、丙、丁四个车间排放的废水中,主要成分分别含有CuCl2、HCl、Na2CO3、NaOH中的一种.从环保角度考虑,该厂决定综合处理废水:通过调节废水流量,使乙、丁两车间废水相对过量,最终排出的溶液呈中性.处理过程如图所示.请回答: 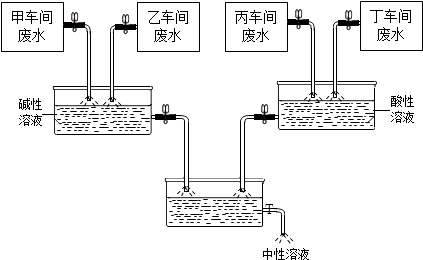
(1)甲、丙、丁三车间排放的废水中,主要成分是:甲车间: , 丙车间: , 丁车间 .
(2)用来检测最终排出的溶液已呈中性.
(3)请具体说明在处理过程中,乙车间和丁车间排出的废水相对过量的目的是: .
【答案】
(1)CuCl2;Na2CO3;HCl
(2)pH试纸(或其他合理的方法)
(3)为了分别除尽废水中的CuCl2或Na2CO3(或Cu2+或CO32﹣)
【解析】解:(1)甲乙反应后的溶液显碱性,乙车间的废水相对过量,所以甲就是氯化铜,乙就是氢氧化钠,丙丁反应后的溶液显酸性,丁车间的废水过量,所以丙是碳酸钠,丁是盐酸,氢氧化钠和碳酸钠不能互换,因为使乙、丁两车间废水相对过量,丙和丁的反应就不会出现酸性,所以答案是:CuCl2;Na2CO3;HCl;(2)在实验室可以用PH试纸测定溶液的PH值,确定酸碱性,所以答案是:pH试纸,(3)氢氧化钠过量可以将铜离子除完,盐酸过量可以将碳酸根离子除完,所以答案是:为了分别除尽废水中的CuCl2或Na2CO3(或Cu2+或CO32﹣)答案:(1)CuCl2;Na2CO3;HCl;(2)pH试纸(或其他合理的方法)(3)为了分别除尽废水中的CuCl2或Na2CO3(或Cu2+或CO32﹣).

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】实验与探究是化学学习的重要方法和内容.
(1)今年5月,我校进行了实验操作考查.小张同学进行的实验考查是“用稀盐酸鉴别氢氧化钠(NaOH)溶液和碳酸钠(Na2CO3)溶液,并测定碳酸钠溶液的pH”.
①小张同学的实验记录如下表,请补充完整:
操作步骤 | 现象记录 | 反应的化学方程式 |
取两支试管,分别往试管中加入2mL样品,再往其中滴入盐酸 | 样品1:无明显现象 | |
样品2: |
②小张用pH试纸测定碳酸钠溶液的酸碱度时,先将试纸用蒸馏水湿润,再将被测试液滴在试纸上.你认为他的做法是否正确?
(2)在实验台上有三瓶未贴标签的溶液,已知分别是硫酸钠溶液、氢氧化钡溶液和稀盐酸.为区别这三种溶液,在老师指导下,兴趣小组的同学把这三种溶液按A、B、C进行编号,然后分别各取适量作为样品加入到三支试管中,进行了如图所示的探究活动: 
【步骤一】中:A、B溶液的颜色无变化,C溶液变成红色;
【步骤二】中:滴入A后溶液的颜色由红色变成无色.当恰好变成无色时,溶液中含有的溶质主要是(酚酞除外).滴入B后,溶液仍显红色,且出现 .
①根据上述实验现象可知,B、C溶液分别是、 .
②实验结束后,该小组的同学欲将废液直接倒入下水道,老师迅速制止.请你解释原因: .