题目内容
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
(1)配制200 g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为______g,水的体积为________mL(水和溶液的密度近似看作1 g/cm3)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的________盘,称量其质量。然后________________________________________________________________________
(按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中
B.按需要添加砝码、移动游码
该步骤中用烧杯而不用纸称量氢氧化钠的原因是______________________。
③溶解:用量筒量取所需体积的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(2)下图表示用上述配制的氢氧化钠溶液与20 g某稀盐酸发生反应后溶液温度的变化情况。
①根据曲线判断,当加入氢氧化钠溶液的质量为________时,反应恰好完全进行。
②当加入15 g氢氧化钠溶液时,所得溶液中的溶质为______________________(写化学式)。

③试计算该稀盐酸的质量分数。(请写出计算过程,反应方程式为:NaOH+HCl===NaCl+H2O)
(1)①16 184
②左 BA 氢氧化钠易潮解(或氢氧化钠具有腐蚀性)
(2)①20 g ②HCl、NaCl
③解:20 g氢氧化钠溶液中NaOH的质量:20 g×8%=1.6 g。
设该稀盐酸中HCl的质量为x。
HCl + NaOH===NaCl+H2O
36.5 40
x 1.6 g
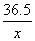 =
=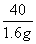
解得x=1.46 g
稀盐酸的质量分数: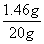 ×100%=7.3%
×100%=7.3%
答:略。