题目内容
5. 化学兴趣小组的同学们用下列药品探究影响金属与酸反应速率的因素.装置中产生氢气的量可以用压强传感器测出(在等温条件下,产生氢气体积与装置内压强成正比.反应放热忽略不计)
化学兴趣小组的同学们用下列药品探究影响金属与酸反应速率的因素.装置中产生氢气的量可以用压强传感器测出(在等温条件下,产生氢气体积与装置内压强成正比.反应放热忽略不计)药品:纯锌片、粗锌片、镁片、5%的稀盐酸、10%的稀盐酸、15%的稀盐酸.
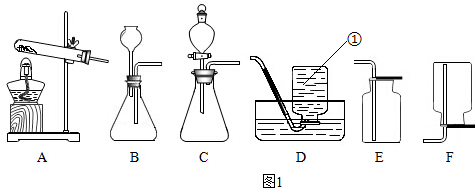
(1)a仪器的名称是锥形瓶;
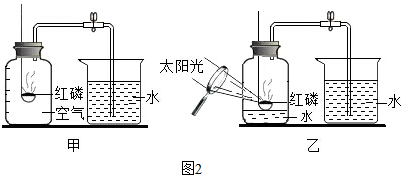
(2)图甲中金属片为镁片,加入盐酸后发生反应的化学方程式为Mg+2HCl=MgCl2+H2↑;
(3)图乙测量的是相同的纯锌片与不同浓度的稀盐酸反应时装置内压强与反应时间的变化关系曲线.你认为该实验要控制的变量还有温度和锌片的质量;从图中可以得出的结论:盐酸浓度越大,反应程度越剧烈;
(4)用稀盐酸与活泼金属反应制取氢气混入氯化氢气体,只要将生成的气体通入氢氧化钠溶液就可以除去混入的该气体;
(5)图丙是足量的相同颗粒大小的纯锌片、粗锌片、镁条分别与5毫升10%的稀盐酸反应过程中装置内压强与反应时间的变化曲线图,从图中你能得出反应物的量与生成氢气量的关系是盐酸完全反应后,生成氢气的质量相等;
(6)由图丙你得出的影响金属与酸反应速率的因素有金属的纯度、金属的种类;
(7)影响金属与酸反应速率还有哪些?请选择一种因素,设计实验证明(可另选药品):
影响因素温度;
实验方案实验步骤:把质量相同、形状相同的镁片、足量的质量分数相同的稀盐酸分别放入装置甲中,其中一个装置放入80℃的水浴装置中;
实验现象:单位时间内,水浴装置中的反应产生的压强大;
实验结论:温度越高,反应速率越快.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)镁和稀盐酸反应生成氯化镁和氢气;
(3)根据盐酸的浓度不同分析解答;
(4)根据氢氧化钠能与盐酸反应解答;
(5)根据最终生成氢气的质量相等解答;
(6)分局所用金属的纯度不同、金属的种类不同解答;
(7)根据影响金属与酸反应速率的因素可能是温度解答,设计实验时要注意控制变量.
解答 解:(1)a仪器的名称是锥形瓶;故填:锥形瓶;
(2)镁和盐酸发生反应的化学方程式为 Mg+2HCl=MgCl2+H2↑;故填:Mg+2HCl=MgCl2+H2↑;
(3)相同的纯锌片与不同浓度的稀盐酸反应,该实验要控制的变量还有温度和锌片的质量;从图中可以看出:盐酸浓度越大,反应程度越剧烈;故填:锌片的质量;盐酸浓度越大,反应程度越剧烈;
(4)氢氧化钠能与盐酸反应,故用稀盐酸与活泼金属反应制取氢气混入氯化氢气体时,可以将生成的气体通入氢氧化钠溶液就可以除去混入的该气体;故填:氢氧化钠;
(5)足量的相同颗粒大小的纯锌片、粗锌片、镁条分别与5毫升10%的稀盐酸反应,从图中可以看出,盐酸完全反应后,生成氢气的质量相等;故填:盐酸完全反应后,生成氢气的质量相等;
(6)图丙实验中,所用的金属的纯度不同、金属的种类不同,故可以看出影响金属与酸反应速率的因素有金属的纯度、金属的种类;故填:金属的纯度;金属的种类;
(7)影响金属与酸反应速率的因素可能是温度,可以取同样的金属镁,与同样的足量的稀盐酸分别放入装置甲中,其中一个装置放入80℃的水浴装置中;用压强传感器测出装置内产生氢气的量,然后得出结论;
故填:温度;
实验步骤:把质量相同、形状相同的镁片、足量的质量分数相同的稀盐酸分别放入装置甲中,其中一个装置放入80℃的水浴装置中;
实验现象:单位时间内,水浴装置中的反应产生的压强大;
实验结论:温度越高,反应速率越快.
点评 本考点主要考查了影响金属与酸发生化学反应速率的因素的探究,还考查了在生产、生活及实验中应注意的问题,从酸的浓度、金属的活动性和金属的状态等不同的角度,设计实验,也考查了学生的实验设计能力.要认真分析,综合把握,问题就会迎刃而解.本考点主要出现在实验题中.

| A. | 把实验剩余的药品倒入废液缸 | |
| B. | 用药匙取用食用盐,再用同一药匙直接取用碳酸钠粉末 | |
| C. | 取用较多量液体药品时,可直接向试管中倾倒 | |
| D. | 向试管中倾倒液体时,试管要直立 |
| 实验 编号 | 温度 | 盐酸 浓度 | 铝片消失的时间/s |
| ① | 20℃ | 5% | 60 |
| ② | 20℃ | 10% | 42 |
| ③ | 40℃ | 10% | 30 |
(2)小明设计实验组合①②的目的是探究稀盐酸的浓度对反应的影响;实验组合②③的目的是探究溶液的温度对反应速率的影响;本实验的结论是反应的温度越高反应越快.
(3)除了用铝片消失的时间来衡量反应的快慢,还可以用反应中冒出的气体的速率方法来衡量反应的快慢.
(4)小明将稀盐酸换成稀硫酸继续实验,发现铝丝和稀硫酸反应现象不明显.
【发现问题】为什么铝丝易与稀盐酸反应而难与稀硫酸反应呢?
【提出假设】Cl-的存在使酸和铝的反应容易进行.
【设计实验】如果你能帮助小明设计一个合理的实验来验证假设取两支试管,分别加入相同的铝丝,然后分别加入等量的稀硫酸,在其中一支试管中加入一定量的氯化钠溶液,观察到加入氯化钠的试管中产生气泡的速度大,说明Cl-的存在使酸和铝的反应容易进行.
(1)催化剂MnO2的用量对反应速率有没有影响呢?
他做了这样一组实验:每次均用30mL10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2用量(克) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(秒) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
答:有影响.在一定范围内,二氧化锰的用量越大,反应越快.
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
| 实验次序 | H2O2溶液溶质质量分数 | MnO2粉末用量(克) | 收集540mL气体所用时间 | 反应后液体温度(℃) |
| 1 | 1% | 0.2 | 660秒 | 24 |
| 2 | 3% | 0.2 | 220秒 | 34 |
| 3 | 5% | 0.2 | 205秒 | 39 |
| 4 | 10% | 0.2 | 80秒 | 56 |
| 5 | 15% | 0.2 | 25秒 | 65 |
| 6 | 20% | 0.2 | 9秒 | 67 |
| 7 | 25% | 0.2 | 4秒 | 69 |
| 8 | 30% | 0.2 | 3秒 | 70 |
答:有影响.过氧化氢溶液的溶质质量分数越大,反应越快.
由表中数据还可看出,该反应是个放热反应(填“放热”或“吸热”).
(3)还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想:二氧化锰颗粒大小(环境温度、气压、是否振荡等).
| A. | 硬水 | B. | 自来水 | C. | 蒸馏水 | D. | 矿泉水 |
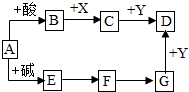 如图是初中化学中常见物质的转化关系(反应条件和部分产物已略去),其中A为钠盐,X、Y均为黑色粉末,D为红色金属单质,F在常温下为液态.试回答下列问题.
如图是初中化学中常见物质的转化关系(反应条件和部分产物已略去),其中A为钠盐,X、Y均为黑色粉末,D为红色金属单质,F在常温下为液态.试回答下列问题.