题目内容
7.现有A、B、C、D、E、F、G、H、I、J十种初中化学常见物质,有如下图所示转化关系.其中A是磁铁矿的主要成分,B、D、E是常见气体,且B和D含有相同的元素,C是应用最广泛的金属,F是红色金属,G是白色沉淀,试剂乙是蓝色溶液,J是一种绿色粉末状固体,它们之间存在如图关系: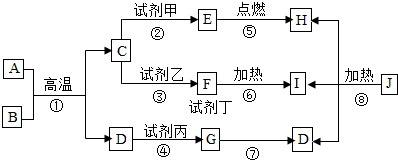
(1)写出下列物质的化学式:FCu,GCaCO3;
(2)反应①的化学方程式为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
(3)反应⑤的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(4)反应⑧的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
分析 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,根据叙述的关键,以及物质的性质和物质之间的反应,做出判断,A是磁铁矿的主要成分,则A是四氧化三铁,B和D是气体,则B可能为一氧化碳,D可能为二氧化碳,生成的C为铁,J是一种绿色粉末状固体,则J可能为碱式碳酸铜,受热能分解生成水,氧化铜和二氧化碳,F是一种红色固体单质,加热能生成I,则F可能为铜,I可能为氧化铜,H可能为水,E点燃能生成水,则E可能为氢气,试剂甲可能为盐酸,铁能与试剂乙反应生成铜,则乙可能是硫酸铜,G是一种不溶于水的白色固体,则G可能是碳酸钙,二氧化碳能与丙反应生成碳酸钙,则丙可能是氢氧化钙,代入框图,推断合理.
解答 解:(1)A是磁铁矿的主要成分,则A是四氧化三铁,B和D是气体,则B可能为一氧化碳,D可能为二氧化碳,生成的C为铁,J是一种绿色粉末状固体,则J可能为碱式碳酸铜,受热能分解生成水,氧化铜和二氧化碳,F是一种红色固体单质,加热能生成I,则F可能为铜,I可能为氧化铜,H可能为水,E点燃能生成水,则E可能为氢气,试剂甲可能为盐酸,铁能与试剂乙反应生成铜,则乙可能是硫酸铜,G是一种不溶于水的白色固体,则G可能是碳酸钙,二氧化碳能与丙反应生成碳酸钙,则丙可能是氢氧化钙,所以本题答案为:Cu,CaCO3;
(2)一氧化碳能与四氧化三铁反应生成二氧化碳和铁,所以本题答案为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;
(3)氢气和氧气反应生成水,所以本题答案为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(4)碱式碳酸铜受热能分解生成氧化铜、水和二氧化碳,所以本题答案为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
点评 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.

| A. | 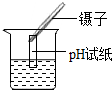 测量溶液的pH | B. | 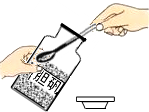 取用固体药品 | C. | 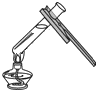 加热液体药品 | D. | 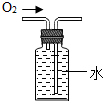 收集氧气 |
| A. | 铁丝在氧气中燃烧:4Fe+3O2 $\frac{\underline{\;点燃\;}}{\;}$ 2Fe2O3 | |
| B. | 铁投入稀盐酸中:2Fe+6HCl═2FeCl3+3H2↑ | |
| C. | 铝片投入硫酸铜:Al+CuSO4═AlSO4+Cu | |
| D. | 高炉炼铁:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 |
| A. | 必须选择含氧的物质作原料 | B. | 必须用排水法收集氧气 | ||
| C. | 必须使用催化剂 | D. | 酒精灯不是一定要用 |
| A. | 煤气燃烧 | B. | 铁锅生锈 | C. | 冷水烧开 | D. | 蔬菜腐烂 |
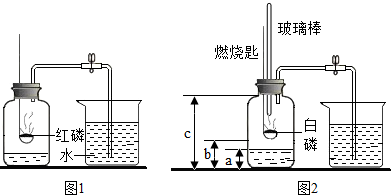
 称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题: