题目内容
某补钙剂标签上对所含的成分有如下说明:每片含主要成分碳酸钙1.5g(相当于钙600mg)。某同学要探究该钙片的主要成分含量是否准确,他取出10片钙片,加入足量的稀盐酸,充分反应,收集到6.6g二氧化碳(假定其它成分不与盐酸反应)。试计算:
(1)每片含碳酸钙的质量是多少?
(2)每片含钙元素的质量是多少?
(3)通过计算,你得出什么结论?
(1)每片含碳酸钙的质量是1.5g;(2)每片含钙元素的质量分数是20%;(3)该钙片的主要成分含量准确.
【解析】
试题分析:【解析】
(1)设10片钙片含碳酸钙的质量为x,
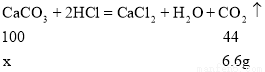

x=15g
(2)每片含碳酸钙的质量为15g÷10=1.5g.每片含钙的质量为1.5g×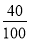 ×100%=0.6g=600mg;
×100%=0.6g=600mg;
③由标签信息,每片含碳酸钙1.5g(相当于钙600mg),与计算结果相符,故该钙片的主要成分含量准确.
答:①每片含碳酸钙的质量是1.5g;②每片含钙元素的质量分数是20%;③该钙片的主要成分含量准确.
考点:元素的质量分数计算;化学方程式的计算.
点评:此题考查化学方程式的计算,关键是从题干中提取信息,解题过程中注意格式的规范化以及计算的准确性.

| A、有水、气体或沉淀生成的反应一定是复分解反应 |
| B、生成盐和水的反应一定是中和反应 |
| C、能与酸反应生成盐水的氧化物一定是碱性氧化物 |
| D、置换反应中一定会发生元素化合价的改变 |
| A、紫色石蕊试液 |
| B、pH试纸 |
| C、无色酚酞试液 |
| D、Na2CO3溶液 |
(9分)为研究化学反应前后反应物与生成物之间的质量关系.
【提出假设】假设一:化学反应中,反应物与生成物的质量相等;
假设二:化学反应中,反应物的质量小于生成物的质量;
假设三:________________________________________.
【实验设计】
实验Ⅰ:称量铁丝,在装有氧气的集气瓶中点燃铁丝,待反应结束后,再称量固体质量.
实验Ⅱ:将装有氢氧化钠溶液的试管放入盛有硫酸铜溶液的烧杯中,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉淀和硫酸钠生成),过一会儿再称量.数据见下表:
编 号 | 实验Ⅰ | 实验Ⅱ |
反应前 | m1g | ag |
反应后 | m2g(大于m1g) | ag |
【实验结论】
甲同学结论为:由实验Ⅰ可知假设2成立;
乙同学结论为:由实验Ⅱ可知假设1成立。
【分析评价】
(1)你认为________(填“甲”、“乙”)同学的结论正确.
(2)实验Ⅰ反应前的质量是_________的质量,增加的质量是_________的质量.
(3)这两个实验中,实验_________正确地反映了反应物与生成物之间的质量关系.说明另一实验设计的不恰当之处__________________________.
(4)在比较反应物或生成物的质量时,应包括参加反应或生成的__________的质量,否则会得出错误结论.
为了测定某纯碱样品中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应,有关实验数据如下表。
反应前 | 反应后实验数据 | ||
烧杯和稀盐酸的质量/g | 120 | 烧杯和其中混合物的质量/g | 127.6 |
纯碱样品的质量/g | 12 | ||
请计算:(1)该反应生成二氧化碳的质量为 g。(2分)
(2)该纯碱样品中碳酸钠的质量分数为多少。(7分)(请写出计算过程)