题目内容
20.等质量的不同金属与足量的稀盐酸反应产生氧气的图象如下,根据图象可知: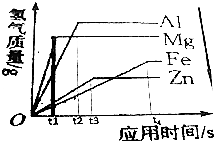
(1)金属活动性顺序:镁>铝>锌>铁
(2)反应时间越短,产生氢气的速度越快,金属越活泼
(3)t1时刻,产生氢气的质量:镁>铝>锌>铁,t4时刻,产生氢气的质量:铝>镁>铁>锌.
分析 镁比铝活泼,铝比锌活泼,锌比铁活泼;
根据图中提供的信息可以判断相关方面的问题.
解答 解:(1)由图中信息可知,反应时间由短到长的分别是镁、铝、锌、铁,即金属活动性顺序是镁>铝>锌>铁.
故填:镁>铝>锌>铁.
(2)反应时间越短,产生氢气的速度越快,金属越活泼.
故填:活泼.
(3)由图中信息可知,t1时刻,产生氢气的质量大小关系是镁>铝>锌>铁;
t4时刻,产生氢气的质量大小关系是铝>镁>铁>锌.
故填:镁>铝>锌>铁;铝>镁>铁>锌.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
11.下列物质的分类中不正确的是( )
| A. | 单质:硅、水银、金刚石 | |
| B. | 碱:烧碱、消石灰、纯碱 | |
| C. | 盐:硝酸银、氯化铁、高锰酸钾 | |
| D. | 氧化物:氧化镁、三氧化硫、五氧化二磷 |
8.如图的反应中,甲、乙、丙三种分子的个数比为1:3:2,则从图示中获得的信息正确的是( )
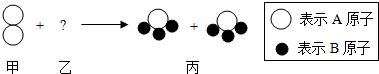

| A. | 反应前后各元素化合价不变 | B. | 原子种类在化学反应中发生了变化 | ||
| C. | 该反应为化合反应 | D. | 乙分子中A与B的原子个数比为1:2 |
15.固体草酸(H2C2O4)在浓硫酸的催化作用下受热分解成碳的氧化物和水.
某化学课外兴趣小组对碳的氧化物的成分进行了实验探究.
【提出问题】如何通过实验确定碳的氧化物的成分.
【猜想】
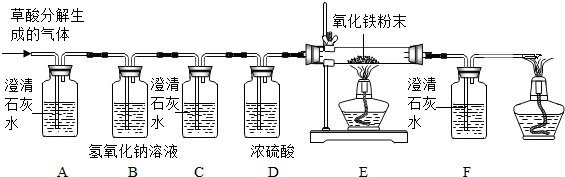
【设计实验】基于猜想3,兴趣小组同学设计了如下实验装置:
【实验探究】
(1)实验过程中观察到A装置(填字母)中的澄清石灰水变浑浊,证明有CO2气体.
(2)实验过程中还观察到以下实验现象:①装置C中澄清石灰水不变浑浊;②E装置中红色粉末变成黑色;③装置F中澄清石灰水变浑浊,证明有CO气体.
【实验结论】通过实验探究证明:猜想3成立.
草酸分解的化学方程式是H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
【问题讨论】
C装置的作用是检验二氧化碳是否已被完全吸收;
E装置发生反应的方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
某化学课外兴趣小组对碳的氧化物的成分进行了实验探究.
【提出问题】如何通过实验确定碳的氧化物的成分.
【猜想】
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | CO和CO2都有 |

【实验探究】
(1)实验过程中观察到A装置(填字母)中的澄清石灰水变浑浊,证明有CO2气体.
(2)实验过程中还观察到以下实验现象:①装置C中澄清石灰水不变浑浊;②E装置中红色粉末变成黑色;③装置F中澄清石灰水变浑浊,证明有CO气体.
【实验结论】通过实验探究证明:猜想3成立.
草酸分解的化学方程式是H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
【问题讨论】
C装置的作用是检验二氧化碳是否已被完全吸收;
E装置发生反应的方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
4.分类是学习化学的方法之一,下列各组物质是按单质、氧化物、混合物进行分类的是( )
| A. | 液氧 水 矿泉水 | B. | 活性炭 火碱 碘盐 | ||
| C. | 生铁 干冰 煤 | D. | 金刚石 熟石灰 空气 |
8.下列属于碱性氧化物的是( )
| A. | CO | B. | P2O5 | C. | CuO | D. | H2O |
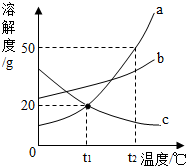 如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题:
如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题: