题目内容
9.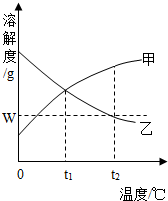 如图是甲、乙的溶解度曲线.在t2℃时向100g水中先后加入w g甲和乙(两种物质溶解时互不影响).充分搅拌.将混合物的温度降低到t1℃.下说法正确的是( )
如图是甲、乙的溶解度曲线.在t2℃时向100g水中先后加入w g甲和乙(两种物质溶解时互不影响).充分搅拌.将混合物的温度降低到t1℃.下说法正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t2℃时,乙溶液溶质质量分数为w% | |
| C. | 温度降低到t1℃时,甲、乙的溶质质量分数相等 | |
| D. | t2℃时,甲物质的溶液为饱和溶液,乙物质的溶液为不饱和溶液 |
分析 根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
饱和溶液溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
溶液中溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液是否饱和.
解答 解:A、温度低于t1℃时,甲的溶解度小于乙的溶解度,温度高于t1℃时,甲的溶解度大于乙的溶解度,温度是t1℃时,甲和乙的溶解度相等,该选项说法不正确;
B、t2℃时,乙的溶解度是wg,在t2℃时向100g水中加入wg乙时恰好饱和,乙溶液溶质质量分数为:$\frac{wg}{100g+wg}$×100%=$\frac{100w}{100+w}$%,该选项说法不正确;
C、在t2℃时向100g水中先后加入wg甲和乙,甲和乙都完全溶解,因此溶质质量分数相等,温度降低到t1℃时,都没有析出固体,因此甲、乙的溶质质量分数相等,该选项说法正确;
D、t2℃时甲的溶解度大于wg,因此甲物质的溶液为不饱和溶液,乙是饱和溶液,该选项说法不正确.
故选:C.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
4.青少年处于生长发育期,需要摄取较多的蛋白质.图中蛋白质含量最高的是( )
| A. |  橙子 | B. |  西红柿 | C. |  大豆 | D. |  玉米 |
14. 已知NaOH容易与空气中的CO2作用而变质.同学们在实验室发现一瓶敞口放置的NaOH固体后,设计方案,对这瓶NaOH固体的变质情况进行了如下实验探究.
已知NaOH容易与空气中的CO2作用而变质.同学们在实验室发现一瓶敞口放置的NaOH固体后,设计方案,对这瓶NaOH固体的变质情况进行了如下实验探究.
【提出问题】:这瓶NaOH一定变质了,其变质程度如何呢?
【实验猜想】:甲同学的猜想:NaOH部分变质.你的新猜想:NaOH全部变质.
【实验探究】:甲同学设计如下实验来验证自己的猜想,请根据表中内容填写空格:
【实验反思】:
(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代甲同学实验中CaCl2溶液的是③④ (填序号).
(2)若将②中加入的溶液换成某盐溶液,会产生与②中不同的实验现象,也可得出中相同的结论.写出一种符合条件的盐的化学式CuSO4或Fe2(SO4)3等.
【探究拓展】为进一步确定原固体的组成,该实验小组的同学称取26.6g待检固体,加入150g稀盐酸恰好完全反应,产生气体质量与稀盐酸的关系如图所示,请计算:
(1)反应生成CO2的质量4.4g;
(2)固体混合物中Na2CO3的质量.
(3)所加稀盐酸的溶质质量分数.
 已知NaOH容易与空气中的CO2作用而变质.同学们在实验室发现一瓶敞口放置的NaOH固体后,设计方案,对这瓶NaOH固体的变质情况进行了如下实验探究.
已知NaOH容易与空气中的CO2作用而变质.同学们在实验室发现一瓶敞口放置的NaOH固体后,设计方案,对这瓶NaOH固体的变质情况进行了如下实验探究.【提出问题】:这瓶NaOH一定变质了,其变质程度如何呢?
【实验猜想】:甲同学的猜想:NaOH部分变质.你的新猜想:NaOH全部变质.
【实验探究】:甲同学设计如下实验来验证自己的猜想,请根据表中内容填写空格:
| 实验步骤 | 现象 | 结论 |
| ①取少量NaOH样品于试管中,加水溶解,滴加足量CaCl2溶液 | NaOH 部分变质 | |
| ②再滴加酚酞 |
(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代甲同学实验中CaCl2溶液的是③④ (填序号).
(2)若将②中加入的溶液换成某盐溶液,会产生与②中不同的实验现象,也可得出中相同的结论.写出一种符合条件的盐的化学式CuSO4或Fe2(SO4)3等.
【探究拓展】为进一步确定原固体的组成,该实验小组的同学称取26.6g待检固体,加入150g稀盐酸恰好完全反应,产生气体质量与稀盐酸的关系如图所示,请计算:
(1)反应生成CO2的质量4.4g;
(2)固体混合物中Na2CO3的质量.
(3)所加稀盐酸的溶质质量分数.
18.化学来源于生活,服务于生活.下列有关化学现象解释正确的是( )
| A. | 厨房做饭厨房外面能闻到,原因是分子在不停地运动 | |
| B. | 盐酸比醋酸酸性强,所以在铝制水壶里装满盐酸并长时间浸泡,除水垢的效果更好 | |
| C. | 铝制品比铁制品耐腐蚀是因为铝的化学性质更稳定 | |
| D. | 电解水时氢气和氧气的体积比为2:1是因为水中氢分子和氧分子的个数比也是2:1 |
19.化学用语是化学学科的语言,在符号5SO3、Mg、H2O中即有微观意义又有宏观意义的符号有( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
 小忻同学称取一定质量的锌粒样品(样品中含有少量不与稀硫酸反应的杂质)放入烧杯中,然后加入100g稀硫酸,恰好完全反应,生成氢气的质量与反应时间的关系如图所示,请回答下列问题:
小忻同学称取一定质量的锌粒样品(样品中含有少量不与稀硫酸反应的杂质)放入烧杯中,然后加入100g稀硫酸,恰好完全反应,生成氢气的质量与反应时间的关系如图所示,请回答下列问题: