题目内容
9.氢气是最轻的气体,难溶于水.氢气作为未来的理想能源,是航天工业的高能燃料,也是化工生产的重要原料.实验室通常采用下面装置制取少量氢气,回答: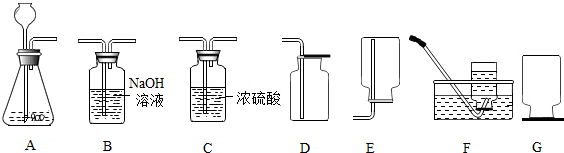
①实验室使用稀盐酸和金属锌制取氢气的化学反应方程式为Zn+2HCl=ZnCl2+H2↑,这种方法制得的氢气往往含有少量氯化氢(原因是盐酸易挥发)和水蒸气,可将杂质气体通过装置B、C除去;
②实验中可采用E、F装置收集氢气;集满氢气后的集气瓶按装置G方式放置备用,原因是氢气比空气轻,防止逸出.
分析 1)从锌与稀盐酸反应生成氯化锌及氢气分析书写方程式,根据B装置中氢氧化钠的性质、浓硫酸具有吸水性分析除掉的杂质;
(2)根据氢气的物理性质特别是密度比空气小以及难溶于水分析判断.
解答 解:(1)锌与稀盐酸反应生成氯化锌和氢气,其方程式为Zn+2HCl=ZnCl2+H2↑;盐酸易挥发,所以这种方法制得的氢气往往含有少量氯化氢和水蒸气,由于B装置中氢氧化钠能与氯化氢反应,所以可除掉气体中的氯化氢气体,浓硫酸具有吸水性,可除去水蒸气;
(2)由于氢气密度比空气小,所以可采用向下排空气法收集,且集满氢气后的集气瓶应倒放到桌面上,氢气难溶于水,所以也可采用排水法收集;
故答案为:(1)Zn+2HCl=ZnCl2+H2↑;氯化氢;盐酸易挥发;B、C;
(2)E、F;氢气比空气轻,防止逸出.
点评 此题是对氢气制取及除杂的考查,解题的关键是掌握相关物质的性质,属基础性知识考查题.

练习册系列答案
相关题目
20.在水溶液中可以大量共存的一组离子是( )
| A. | H+、K+、OH- | B. | Na+、H+、HCO3- | C. | Fe3+、NO3-、OH- | D. | H+、NH4+、Cl- |
17.下列实验方法一定能达到实验目的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 检验气体是否为CO2 | 将气体通入盛有澄清石灰水的试管中 |
| B | 鉴别石灰水和NaOH溶液 | 加入适量的稀盐酸 |
| C | 除净CO中少量的CO2 | 将气体通过盛有澄清石灰水的洗气瓶 |
| D | 比较Zn、Cu、Ag的金属活动性 | 将Zn和Ag分别放入CuSO4溶液中 |
| A. | A | B. | B | C. | C | D. | D |
14.下列物质露置在空气中一段时间后,因为发生了化学变化而使溶液质量增加的是( )
| A. | NaOH溶液 | B. | 浓盐酸 | C. | 浓硫酸 | D. | 石灰水 |
1.把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,测得各物质的质童如表所示
下列说法正确的是( )
| 物 质 | A | B | C | D |
| 反应前质置/g | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
| A. | 反应后密闭容器中A的质量为9.7g | |
| B. | 物质C一定是化合物,物质D可能是单质 | |
| C. | 反应过程中,物质B和物质D变化的质量比为87:36 | |
| D. | 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为1:2 |
19.制作如图物品所用的主要材料中,属于有机合成材料的是( )
| A. |  不锈钢杯 不锈钢杯 | B. |  纯棉毛巾 纯棉毛巾 | ||
| C. |  木桶 木桶 | D. |  涤纶制成的航天服 涤纶制成的航天服 |
