题目内容
8.检查实验室制氧气装置的装置气密性的方法是什么?分析 装置气密性检验的原理是:通过气体发生器与液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏;一般用到的方法有:空气热胀冷缩法、注水法等;据此进行分析解答即可.
解答 解:检查实验室制氧气装置的装置气密性的方法是把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,说明装置不漏气.
故答案为:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,说明装置不漏气.
点评 本题难度不大,装置气密性的检查是常考的实验题,掌握检验装置气密性时可以通过改变体系内的压强是正确解答此类题的关键.

练习册系列答案
相关题目
19.四位同学分别用下列四种方法检验NaOH溶液是否已变质含有Na2CO3,
(1)加少量稀盐酸,无气泡放出,则一定不含Na2CO3
(2)加少量澄清石灰水,有沉淀生成,则一定含有Na2CO3
(3)加少量CaCl2溶液,有沉淀生成,则一定含有Na2CO3
(4)加少量BaCl2溶液有沉淀生成,则一定含有Na2CO3,
其中方法和结论都正确的是( )
(1)加少量稀盐酸,无气泡放出,则一定不含Na2CO3
(2)加少量澄清石灰水,有沉淀生成,则一定含有Na2CO3
(3)加少量CaCl2溶液,有沉淀生成,则一定含有Na2CO3
(4)加少量BaCl2溶液有沉淀生成,则一定含有Na2CO3,
其中方法和结论都正确的是( )
| A. | (1)(2) | B. | (1)(2)(3) | C. | (2)(3)(4) | D. | (1)(2)(3)(4) |
13.以下是某研究小组探究影响反应速率部分因素的相关实验数据.
(1)通过实验①和②对比可知,化学反应速率与浓度有关;
(2)从实验③和④对比可知,化学反应速率与温度的关系是:温度越高,化学反应速率越快;
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量不变. 在此反应中MnO2起催化作用.
(4)该研究小组探究影响反应速率部分因素实验中采用了控制变量的方法.
| 实验序号 | H2O2溶 液浓度% | H2O2溶液体积/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 无 | 2 | 49.21 |
| ④ | 30 | 5 | 55 | 无 | 2 | 10.76 |
(2)从实验③和④对比可知,化学反应速率与温度的关系是:温度越高,化学反应速率越快;
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量不变. 在此反应中MnO2起催化作用.
(4)该研究小组探究影响反应速率部分因素实验中采用了控制变量的方法.
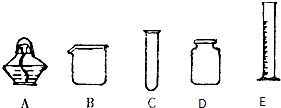 如图仪器中,既能用来配制溶液又能作较大量试剂反应容器的是(填标号)B,用作收集或贮存少量气体的是D,可间接加热的仪器是B,A仪器的名称是酒精灯.
如图仪器中,既能用来配制溶液又能作较大量试剂反应容器的是(填标号)B,用作收集或贮存少量气体的是D,可间接加热的仪器是B,A仪器的名称是酒精灯.