题目内容
1.在实验室用以下装置进行气体的制取实验.
(1)选择装置A用KClO3和MnO2制氧气的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,该装置中试管口略向下倾斜的原因是防止冷凝水回流到热的试管底部炸裂试管,要收集到较纯净的氧气,最好选用装置C(填字母序号).
(2)选择装置B制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,实验时长颈漏斗末端管口应位于液面以下的目的是防止生成的CO2从长颈漏斗逸出,用澄清石灰水检验二氧化碳气体的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.
(3)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置是C(填字母序号).
分析 (1)根据氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,试管口略向下倾斜,防止冷凝水倒流炸裂试管,排水法收集的氧气纯净进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,实验时长颈漏斗末端管口应位于液面以下的目的是防止生成的CO2从长颈漏斗逸出,二氧化碳和氢氧化钙反应会生成碳酸钙沉淀和水进行分析;
(3)根据一氧化氮气体难溶于水,在空气中容易与氧气发生反应进行分析.
解答 解:(1)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,试管口略向下倾斜,防止冷凝水倒流炸裂试管,排水法收集的氧气纯净,所以要收集到较纯净的氧气,最好选用装置C;
(2)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,实验时长颈漏斗末端管口应位于液面以下的目的是防止生成的CO2从长颈漏斗逸出,二氧化碳和氢氧化钙反应会生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(3)一氧化氮气体难溶于水,在空气中容易与氧气发生反应,所以收集装置是C.
故答案为:(1)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,防止冷凝水回流到热的试管底部炸裂试管,C;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑,防止生成的CO2从长颈漏斗逸出,Ca(OH)2+CO2=CaCO3↓+H2O;
(3)C.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
11.下列实验操作正确的是( )
| A. |  滴加液体 | B. |  取用固体 | C. |  测溶液pH | D. |  过滤 |
9.下列实验操作中正确的是( )
| A. |  过滤 | B. |  氧气验满 | C. |  加热液体 | D. |  取用固体粉末 |
6.下列说法正确的是( )
| A. | 凡是含氧元素的化合物都是氧化物 | |
| B. | 物质发生化学反应的同时伴随着能量的变化 | |
| C. | 如果没有二氧化锰做催化剂,过氧化氢就不会分解 | |
| D. | 空气中的氮气、氧气经混合,它们的化学性质都已改变 |
13.下列物质属于纯净物的是( )
| A. | 液氧 | B. | 矿泉水 | C. | 铝合金 | D. | 洁净的空气 |
11.下列实验操作,正确的是( )
| A. |  检查气密性 | B. |  量取液体 | C. | 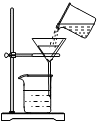 过滤 | D. |  熄灭酒精灯 |
