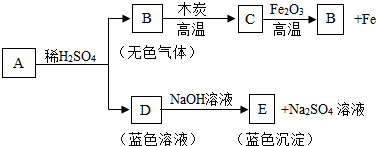
题目内容
13.下表为元素周期表中某一周期元素的原子结构示意图. 请回答下列问题:
请回答下列问题:(1)表中硫原子的核电荷数x=16,在化学反应中容易得到电子.
(2)表中具有相对稳定结构的元素是氩元素(或Ar).
(3)写出铝离子的结构示意图
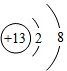 .
.(4)镁元素与氯元素形成的化合物化学式为MgCl2.
(5)上述元素在周期表中处于同一周期的原因是它们的原子核外电子层数相同.
分析 (1)根据元素周期表的信息以及最外层电子数来分析;
(2)最外层具有8个电子的原子具有相对稳定结构;
(3)铝原子最外层有3个电子,在化学变化中易失去3个电子而形成铝离子;
(4)根据化合物的化学式写法来分析;
(5)根据元素周期数与电子层数的关系进行分析解答.
解答 解:(1)在原子中,质子数=核外电子数,x=2+8+6=16,其原子最外层有6个电子,在化学变化中易得到电子,故填:16;得到;
(2)最外层具有8个电子的原子具有相对稳定结构,表中具有相对稳定结构的元素氩元素.故填:氩元素(或Ar);
(3)铝离子的结构示意图为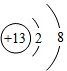 ;故填:
;故填: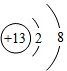 ;
;
(4)在化合物中,镁元素显+2价,氯元素显-1价,故氯化镁的化学式为MgCl2,故填:MgCl2;
(5)由元素周期表中某一周期元素的原子结构示意图可以看出,处于同一周期的原子,核外电子层数相同.故填:它们的原子核外电子层数相同.
点评 本题难度不大,是常考的题型,掌握同一周期的各原子结构示意图的特点、化学式的书写等是正确解答此类题的关键.

练习册系列答案
相关题目
4.归纳与反思是学习化学的重要环节.下列各项归纳完全正确的是( )
| A性质与用途 | B能源与环境 |
| 氧气有助燃性--做燃料 生石灰具有吸水性--用作干燥剂 | 使用氢能源--无污染 使用乙醇汽油--无污染 |
| C物质的鉴别 | D营养与健康 |
| 软水和硬水--肥皂水 聚乙烯和聚氯乙烯--灼烧 | 人体缺维生素C--易患坏血病 人体缺钙--甲状腺肿大 |
| A. | A | B. | B | C. | C | D. | D |
8.市场上销售的食盐有“加碘盐“、“加钙盐“、“加锌盐“,这里的碘、钙、锌是指( )
| A. | 原子 | B. | 离子 | C. | 分子 | D. | 元素 |
18.某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑),这种工业称为“氯碱工业”.某研究性学习小组对该厂生产的烧碱样品进行如下探究.
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】
猜想1:可能含有Na2CO3;
猜想2:可能含有NaCl;
猜想3:可能含有Na2CO3和NaCl.
作出猜想1的依据是2NaOH+CO2═Na2CO3+H2O (用化学方程式表示).
【设计实验】
【交流与讨论】
小坚同学提出:“上述实验II中稀硝酸也可以用稀盐酸代替”.你认为他的观点不正确(填“正确”或“不正确”),理由是引入Cl-,干扰对NaCl的检验.
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】
猜想1:可能含有Na2CO3;
猜想2:可能含有NaCl;
猜想3:可能含有Na2CO3和NaCl.
作出猜想1的依据是2NaOH+CO2═Na2CO3+H2O (用化学方程式表示).
【设计实验】
| 实验步骤 | 实验现象 | 解释或结论 |
| I.取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁. | 试管外壁发热 | 原因是氢氧化钠固体溶于水放热. |
| II.向I所得的溶液中逐滴加入 稀硝酸至过量 | 刚开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体. | 猜想1可能成立. |
| III.向II所得的溶液中滴加几滴硝酸银溶液. | 产生白色沉淀 | 结合实验II,猜想3成立. |
小坚同学提出:“上述实验II中稀硝酸也可以用稀盐酸代替”.你认为他的观点不正确(填“正确”或“不正确”),理由是引入Cl-,干扰对NaCl的检验.
2.下列有关物质的组成与分类说法正确的是( )
| A. | 葡萄糖(C6H12O6)不属于氧化物但属于有机物 | |
| B. | 煤气主要是由一氧化碳、二氧化碳等气体物质组成的混合物 | |
| C. | 红磷、木炭、煤、石油、天然气都属于燃料 | |
| D. | 合金和塑料属于合成材料 |
7.物理变化与化学变化的根本区别是( )
| A. | 发光、发热 | B. | 有气体或沉淀产生 | ||
| C. | 物质的颜色发生改变 | D. | 有没有新物质生成 |