题目内容
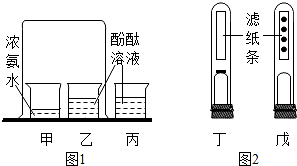
3.如图所示为实验室中常见的制取气体的发生装置和收集装置.
请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用的发生装置是(填字母序号),反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.实验室用过氧化氢溶液和二氧化锰制取氧气,应选用的发生装置是B(填字母序号),反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(2)若使用E收集氧气,判断氧气已收集满的现象是瓶口有有大气泡向外冒出,若使用装置C收集氧气,验证氧气已经收集满的方法是将带火星的小木条放在瓶口,若复燃,则已满;待检验到D中氧气已收集满,接下来的操作是移出导管,然后把集气瓶盖好玻璃片,正放在桌面上.
(3)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置E(填字母序号).
(4)用高锰酸钾制取氧气的实验过程中,马明同学观察到装置E中的水变为红色,这是因为高锰酸钾粉末进入导管的缘故.为了防止实验过程出现上述现象,相应的改进措施是试管口放一小团棉花.
分析 (1)制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.(2)根据收集氧气时的注意事项、验满方法来分析;
(3)根据一氧化氮的性质分析收集的方法及装置.
(4)用高锰酸钾时,试管口要有一团棉花,防止高锰酸钾粉末进入导管.
解答 解:(1)如果用高锰酸钾制氧气就需要加热,选择装置A来制取;实验室用高锰酸钾制取氧气的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,如果用双氧水和二氧化锰制氧气就不需要加热,选择仪器B来制取,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;
故填:A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;B;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)若用排水法收集氧气时,当看到集气瓶口有大气泡向外冒出说明氧气已经收集满了,此时先将导管从水槽中取出,再熄灭酒精灯;用向上排空气法收集氧气时,将一根带火星的木条放在集气瓶口,若观察到木条复燃,证明氧气已满,故填:瓶口有有大气泡向外冒出;将带火星的小木条放在瓶口,若复燃,则已满;移出导管;
(3)由于一氧化氮气体难溶于水,在空气中容易与氧气发生反应,只能用排水法收集,收集装置是:E.故填:E;
(4)观察到E装置中的水变为紫红色,这是因为试管口没有放棉花团,高锰酸钾粉末进入E装置并溶于水中的缘故;因此用高锰酸钾制取氧气时,试管口要有一团棉花;故填:高锰酸钾粉末进入导管;试管口放一小团棉花.
点评 本题主要考查了气体制取装置的选择和连接方法,会根据气体的制取原理来组装、选配、判断或者选择气体的发生装置;再根据气体的溶解性、密度及其是否与水或者空气发生反应等来判断、选用收集装置.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 用二氧化碳灭火器灭火 | B. | 砍掉树木形成隔离带 | ||
| C. | 用锅盖盖灭着火的油锅 | D. | 消防队员用高压水枪灭火 |
| A. | 每个分子由4个碳原子、8个氢原子和2个氧原子构成 | |
| B. | 属于氧化物 | |
| C. | 碳、氢、氧三种元素质量比为6:1:4 | |
| D. | 相对分子质量为88 |
| A. | 铜作导线 | B. | 干冰作制冷剂 | C. | 酒精作燃料 | D. | 活性炭作吸附剂 |
| A. | 氢氧化铜 | B. | 铁丝 | C. | 碳酸钠溶液 | D. | 铜片 |