题目内容
3.碳12原子的质量为1.993×10-26 kg,一种氧原子的质量为2.657×10-26 kg,计算该氧原子的相对原子质量(保留小数点后一位).分析 以一种碳原子质量的$\frac{1}{12}$为标准,其他原子的质量跟它相比较所得到的比,作为这种原子的相对原子质量.
用公式表示为:某原子的相对原子质量=$\frac{该原子的质量}{碳原子的质量×\frac{1}{12}}$,将数据代入公式计算即可.
解答 解:
氧原子的相对原子质量=$\frac{该原子的质量}{碳原子的质量×\frac{1}{12}}$
=$\frac{2.657×1{0}^{-26}kg}{1.993×1{0}^{-26}kg×\frac{1}{12}}$=16.0
故答案为:16.0.
点评 解答有关相对原子质量的计算题时,要注意相对原子质量是一个比值,是原子的实际质量和碳原子质量的$\frac{1}{12}$之比,掌握此知识点就能轻松解题.

练习册系列答案
相关题目
13.下列有关的化学用语表达错误的是( )
| A. | 五个氢原子:5H | B. | 碳酸钠:NaCO3 | ||
| C. | 两个钙离子:2Ca2+ | D. | 一个铵根离子:NH4+ |
14.某化学学习小组的同学辨析以下说法,其中正确的是( )
| A. | 用水灭火时,水降低了可燃物的着火点 | |
| B. | KCl、CuSO4、NaNO3在水中能大量共存 | |
| C. | 中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应 | |
| D. | 某物质在空气中燃烧后生成二氧化碳和水,所以该物质一定含有碳、氢、氧元素 |
8.下列相同质量的金属,原子数目最少的是( )
| A. | Mg | B. | Al | C. | Na | D. | Ca |
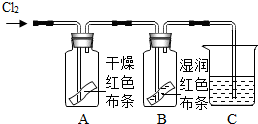 如图是探究物质漂白性(使有色物质褪色)的实验.已知氯气(Cl2)是一种有刺激性气味的有毒气体,
如图是探究物质漂白性(使有色物质褪色)的实验.已知氯气(Cl2)是一种有刺激性气味的有毒气体,


 2013年12月15日,嫦娥三号成功与玉兔号月球车互拍,五星红旗亮相月面.嫦娥三号任务成功实施,使中国成为世界上第三个掌握月球软着陆和月面巡视探测技术的国家.
2013年12月15日,嫦娥三号成功与玉兔号月球车互拍,五星红旗亮相月面.嫦娥三号任务成功实施,使中国成为世界上第三个掌握月球软着陆和月面巡视探测技术的国家.