题目内容
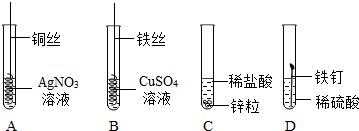
12.如图为某学习小组探究金属化学性质时做出的四个实验,仔细分析后回答下列问题:(1)描述A中的实验现象铜丝表面附着了一层银白色固体,溶液由无色变成蓝色;
(2)写出D中反应的化学方程式Fe+H2SO4═FeSO4+H2↑;
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是AB(填序号).
分析 铜能和硝酸银反应生成硝酸铜和银;
铁能和稀硫酸反应生成硫酸亚铁和氢气;
铁能和硫酸铜反应生成硫酸亚铁和铜.
解答 解:(1)A中铜和硝酸银反应生成硝酸铜和银,能够观察到铜丝表面附着了一层银白色固体,溶液由无色变成蓝色.
故填:铜丝表面附着了一层银白色固体,溶液由无色变成蓝色.
(2)D中铁能和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
故填:Fe+H2SO4═FeSO4+H2↑.
(3)要证明Cu、Fe、Ag的活动性顺序,通过A证明铜比银活泼,通过B证明铁比铜活泼,因此至少要做的实验是AB.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
1.某溶液中存在Na+、Fe3+、SO42-三种离子,其个数比一定不成立的是( )
| A. | 1:1:2 | B. | 1:3:5 | C. | 1:5:8 | D. | 1:7:10 |
4.下列实验操作正确或实验数据合理的是( )
| A. | 用托盘天平称量固体时,应将药品放在右盘上,砝码放在左盘上 | |
| B. | 将试剂瓶中的液体倒入试管中,必须用漏斗引流 | |
| C. | 用排水法收集满氧气的集气瓶在水下用玻片盖好,再取出正立于桌面上 | |
| D. | 用10mL量筒准确量取了6.53mL水 |