题目内容
13.在一密闭容器中有X、Y、Z、Q四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如下表.则:| 物质 | X | Y | Z | Q |
| 反应前物质质量/g | 2 | 2 | 84 | 5 |
| 反应后物质质量/g | 待测 | 24 | 0 | 14 |
(2)反应后测得容器中X的质量为55g.
(3)参加反应的各物质的质量比为53:22:9.
分析 本题可分析Y、Z、Q三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定X是反应物还是生成物,进而可以确定反应类型.
解答 解:(1)由表中数据分析可知,反应前后,Y的质量增加了24g-2g=22g,故Y是生成物,生成的Y的质量为22g;同理可以确定Z是反应物,参加反应的Z的质量为84g-0g=84g;Z的质量增加了14g-5g=9g,故Z是生成物,生成的Z的质量为9;由质量守恒定律,X应是生成物,且生成的X的质量为84g-22g-9g=53g,故待测的数53g+2g=55g.该反应的反应物为X、Y、Q,生成物是Z,符合“多变一”的特征,属于化合反应.
(2)反应后测得容器中X的质量为55g.
(3)参加反应的各物质的质量比为53g:22g:9g=53:22:9.
故答案为:(1)化合反应;(2)55g;(3)53:22:9.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.

练习册系列答案
相关题目
3.推动污染减排、建设环境友好型社会是全社会共同的责任.下列物质中,属于大气主要污染物,必须减少排放的是( )
| A. | 二氧化硫 | B. | 水蒸气 | C. | 氮气 | D. | 氧气 |
4.下列变化属于物理变化的是( )
| A. | 食物变质 | B. | 钢铁生锈 | C. | 水材燃烧 | D. | 玻璃破碎 |
8.下列物质的名称与化学符号对应错误的是( )
| A. | 木炭-C | B. | 水-H2O | C. | 五氧化二磷-O5P2 | D. | 二氧化硫-SO2 |
3.研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的过程:
【假设】H2O2生成O2的快慢与催化剂种类有关.
实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间.
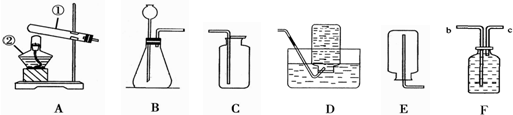
【进行实验】图丁是他们进行实验的装置图,气体发生装置中A仪器的名称是锥形瓶,此实验中B处宜采用的气体收集方法是排水法.
【实验记录】
【结论】该探究过程得出的结论是相同条件下H2O2生成O2的快慢与催化剂的种类有关.
【反思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快.若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的质量和化学性质是否改变.
【实验拓展】H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
【假设】H2O2生成O2的快慢与催化剂种类有关.
实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间.
【进行实验】图丁是他们进行实验的装置图,气体发生装置中A仪器的名称是锥形瓶,此实验中B处宜采用的气体收集方法是排水法.
【实验记录】
| 实验编号 | 1 | 2 |
| 反应物 | 5% H2O2 | 5%H2O2 |
| 催化剂 | 1g水泥块 | 1g二氧化锰 |
| 时间 | 165s | 46s |
【反思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快.若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的质量和化学性质是否改变.
【实验拓展】H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
| 实验步骤 | 现 象 | 结 论 |
| 取一支试管加入3mL5%的过氧化氢溶液,然后加入少量二氧化锰. | 缓慢有少量气泡冒出 | 浓度越大,过氧化氢分解的速率越快 |
| 另取一支试管加入3mL15%的过氧化氢溶液,然后加入少量二氧化锰. | 迅速有大量气泡冒出 |
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
| 实验步骤 | 现 象 | 结 论 |
| 取一支试管加入5mL 15%的过氧化氢溶液.然后把试管放入盛有冷水的烧杯中; 取一支试管加入5mL 15%的过氧化氢溶液.然后把试管放入盛有热水的烧杯中 | 缓慢有少量气泡冒出; 迅速有大量气泡冒出 | 温度越高,过氧化氢分解的速率越大 |