题目内容
3.元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息.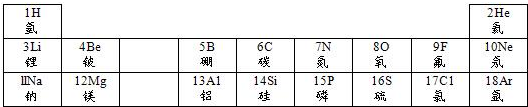
(1)地壳中含量仅次于氧的非金属元素名称是硅,该元素原子的质子数为14
(2)
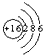 所表示的粒子符号为S,他的最外层电子数为6
所表示的粒子符号为S,他的最外层电子数为6(3)由原子序数为11和17的两种元素组成的化合物是NaCl(写化学式).
(4)从11-17,随着原子序数的增加,其原子结构(或元素的性质)呈现出的变化规律是随着原子序数的增加,元素原子的最外层电子数逐渐增加(任写一条)
分析 (1)根据地壳中各元素含量解答;
(2)根据原子结构示意图各部分含义解答;
(3)根据化合物的化学式的写法来分析;
(4)从元素的原子结构示意图可判断出原子序数的递增与其原子结构的关系.
解答 解:(1)地壳中元素含量由高到低的顺序是氧、硅、铝、铁,仅次于氧的非金属元素名称是硅,硅原子的质子数为14;故填:硅;14;
(2)图中粒子质子数为16,核外电子数为16,为硫原子,符号为S;最外层上有6个电子;故填:S;6;
(3)在化合物中,钠元素显+1价,氯元素显-1价,二者组成的化合物是氯化钠,故填:NaCl;
(4)从题目中给出的11-17号元素的原子结构示意图可看出,随原子序数的递增,原子结构呈现的变化规律是:随着原子序数的增加,元素原子的最外层电子数逐渐增加,故填:随着原子序数的增加,元素原子的最外层电子数逐渐增加.
点评 此题主要考查元素周期表、原子结构示意图的意义,原子和离子的转化,化学式的书写以及随原子序数的递增原子结构的变化规律,属于中等难度的题型.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列实验方案正确的是C
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去硫酸镁溶液中的硫酸 | 加入过量的Ba(OH)2溶液,过滤 |
| B | 分离氯化钠和硝酸钠固体混合物 | 加水溶解后,过滤,蒸发结晶 |
| C | 鉴别氯化铵和氯化钙 | 分别加入熟石灰,研磨,闻气味 |
| D | 鉴别羊毛织物和涤纶织物 | 分别灼烧,闻气味 |
8.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如表
请回答下列问题:
(1)请根据质量守恒定律判断X的值是D
A、50 B、40 C、20 D、10
(2)甲一定(填“一定”或“不一定”,下同)是反应物;丁不一定 是催化剂.
(3)该反应属于化合(填“化合”或“分解”)反应.
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量(g) | 20 | 50 | 80 | 30 |
| 反应后的质量(g) | 0 | 140 | X | 30 |
(1)请根据质量守恒定律判断X的值是D
A、50 B、40 C、20 D、10
(2)甲一定(填“一定”或“不一定”,下同)是反应物;丁不一定 是催化剂.
(3)该反应属于化合(填“化合”或“分解”)反应.
15.在一密封容器内有X、Y、Z、Q四种物质,在一定条件下充分反应后,测得反应后各物质的质量如表:
(1)反应后测得容器中物质X的质量为:55;
(2)该容器中发生的化学反应其本类型为:分解反应;请写一个和该反应类型相同的化学反应方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)该反应中物质Z与X的质量比为:84:53.
| 物质 | X | Y | Z | Q |
| 反应前质量 | 2 | 2 | 84 | 5 |
| 反应后质量 | 待测 | 24 | 0 | 14 |
(2)该容器中发生的化学反应其本类型为:分解反应;请写一个和该反应类型相同的化学反应方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)该反应中物质Z与X的质量比为:84:53.
12.下列物质属于氧化物的是( )
| A. | O2 | B. | CuO | C. | H2SO4 | D. | NaOH |
13.下列有关酒精灯的操作,错误的是( )
| A. | 用燃烧的酒精灯引燃另一只酒精灯 | |
| B. | 酒精灯用灯帽盖灭,不可用嘴吹灭 | |
| C. | 绝对禁止向燃着的酒精灯里添加酒精 | |
| D. | 用火柴点燃酒精灯 |
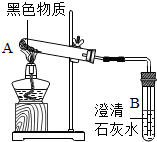 镁是一种银白色有金属光泽的金属.但实验时见到镁条总有一层灰黑色的“外衣“,这层灰黑色物质是什么呢?
镁是一种银白色有金属光泽的金属.但实验时见到镁条总有一层灰黑色的“外衣“,这层灰黑色物质是什么呢?