题目内容
18.下列各组离子能在pH=1水溶液中大量共存且无色的溶液是( )| A. | Ag+、Cl-、Fe2+、NO3- | B. | CO32-、K+、Ca2+、Cl- | ||
| C. | Cu2+、OH-、SO42-、Ba2+ | D. | NH4+、NO3-、Na+、Cl- |
分析 pH为1的水溶液显酸性,水溶液中含有大量的H+.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存;本题还要注意溶液呈无色,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:pH为1的水溶液显酸性,水溶液中含有大量的H+.
A、Ag+、Cl-能结合生成不溶于酸的氯化银沉淀,不能大量共存,且Fe2+的水溶液呈浅绿色,故选项错误.
B、CO32-和H+在溶液中能结合生成水和二氧化碳,不能大量共存,故选项错误.
C、SO42-、Ba2+能结合生成不溶于酸的硫酸钡沉淀,不能大量共存,OH-与H+在溶液中能结合生成水,且Cu2+的水溶液呈蓝色,故选项错误.
D、四者之间不反应,能在酸性溶液中共存,且不存在有色离子,故选项正确.
故选:D.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;还要注意是在酸性溶液中共存及特定离子的颜色.

练习册系列答案
相关题目
8.杂卤石(K2SO4•MgSO4•2CaSO4•2H2O)属于“呆矿”,为能充分利用钾资源,用饱和的Ca(OH)2溶液浸杂卤石制备硫酸钾,工艺流程如下:
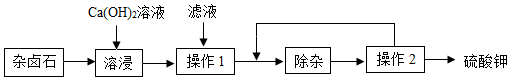
已知:
(1)操作1的名称为过滤,所需的玻璃仪器有玻璃棒、烧杯、漏斗,玻璃棒的作用是引流.
(2)滤渣的主要成分有Mg(OH)2和CaSO4.
(3)“除杂”环节中,先加入a溶液(填字母,下同),经搅拌等操作后,过滤,再加入
c溶液调滤液pH至中性.
a.K2CO3 b.Na2CO3 c.稀硫酸 d.稀盐酸
(4)操作2的步骤是蒸发浓缩、降温结晶、过滤、洗涤.
(5)洗涤硫酸钾最好选用c.
a.30℃的水 b.饱和的硫酸钠溶液 c.饱和的硫酸钾溶液.

已知:
| 物质 | CaSO4 | K2SO4 | Mg(OH)2 |
| 溶解度/g(25℃) | 0.28 | 11.1 | 0.00084 |
(2)滤渣的主要成分有Mg(OH)2和CaSO4.
(3)“除杂”环节中,先加入a溶液(填字母,下同),经搅拌等操作后,过滤,再加入
c溶液调滤液pH至中性.
a.K2CO3 b.Na2CO3 c.稀硫酸 d.稀盐酸
(4)操作2的步骤是蒸发浓缩、降温结晶、过滤、洗涤.
(5)洗涤硫酸钾最好选用c.
a.30℃的水 b.饱和的硫酸钠溶液 c.饱和的硫酸钾溶液.
6.生活中处处有化学,下列家庭小实验中不涉及化学变化的是( )
| A. |  柠檬酸、纯碱等制汽水 | B. |  木炭除去冰箱中异味 | ||
| C. |  食醋除去水垢 | D. |  探究铁生锈的条件 |
13.2017年1月27日,南京理工大学胡炳成教授团队成功合成世界首个全氮阴离子盐(N3-),全氮类超高含能材料(炸药)的能量可达3倍TNT以上(爆炸产物为氮气).下列说法中不正确的是( )
| A. | N3-是氮元素的一种新单质 | |
| B. | N3-是带一个单位负电荷的阴离子 | |
| C. | 全氮类超高含能材料爆炸的产物无污染 | |
| D. | 氮气的化学性质很稳定 |
3.下列图示的实验操作中错误的是( )
| A. |  气密性的检查 气密性的检查 | B. | 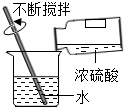 稀释浓硫酸 稀释浓硫酸 | ||
| C. |  铁丝在氧气中燃烧 铁丝在氧气中燃烧 | D. |  测定空气的组成 测定空气的组成 |
10.日常生活中的下列做法,利用了化学变化的是( )
| A. | 用洗衣粉洗去衣服上的油污 | |
| B. | 用酒精杀菌消毒 | |
| C. | 用硫酸钡做钡餐透视 | |
| D. | 用开水烫洗香椿芽去除其含有的亚硝酸盐 |
7.物质的下列用途主要利用其物理性质的是( )
| A. | 干冰用于人工降雨 | B. | 稀盐酸用于金属表面除锈 | ||
| C. | 白醋由于清除水壶中的水垢 | D. | 苏打水用于缓解胃酸过多 |
10.下列物质中,属于溶液的是( )
| A. | 硬水 | B. | 石灰乳 | C. | 冰水 | D. | 液氧 |